Anilin
| Anilin | |
  | |
| Systematiskt namn | Fenylamin |
|---|---|
| Övriga namn | Aminobensen |
| Kemisk formel | C6H5NH2 |
| Molmassa | 93,1265 g/mol |
| Utseende | Färglös vätska |
| CAS-nummer | 62-53-3 |
| SMILES | Nc1ccccc1 |
| Egenskaper | |
| Densitet | 1,0297 g/cm³ |
| Löslighet (vatten) | 35 g/l (20 °C) |
| Smältpunkt | -6,3 °C |
| Kokpunkt | 184,13 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| LD50 | 871 mg/kg |
| SI-enheter & STP används om ej annat angivits | |
Anilin är en kemisk förening med formeln C6H5NH2. Ämnet är en färglös, mycket giftig och illaluktande olja.
Historia
Anilin framställdes första gången av den tyske kemisten Otto Unverdorben år 1826 genom destillering av naturligt indigo. År 1834 lyckades Friedlieb Ferdinand Runge utvinna "kyanol" eller "blåolja" ur stenkolstjära. Även Nikolaj Zinin lyckades 1842 framställa ämnet "benzidam" ur nitrobenzol, och Carl Julius Fritzsche gav 1841 ämnet, som han liksom Unverdorben lyckats framställa ur indigo namnet anilin efter det portugisiska namnet för indigo, "anil". 1843 kunde O.L. Erdmann och August Wilhelm von Hofmann visa att det rörde sig om samma ämne, och gav det det gemensamma namnet anilin.[1]
Att kunna framställa större mängder till lägre kostnad var dock det stora problemet. Det var först sedan Mansfield 1847 funnit en metod att fabriksmässigt framställa benzol av stenkolstjära, som ämnet blev tillgängligt i större mängder. August Wilhelm von Hofmann hade 1849 länge studerat indigodestillaten, och från 1849 även ammoniaken och dess derivat, och därmed 1855 slutligen lyckades fastställa att det var samma ämne i samtliga fall.[1]
Året efteråt (1856) framställde von Hofmanns student William Perkin färgämnet mauvein av anilin, och 1858 angav von Hofmann en metod för att praktiskt kunna framställa anilinrött. 1861 upptäcktes anilinblått, och därpå anilinviolett och anilingrönt, som von Hofmann visade vara derivat av anilinrött. Från 1870 kom en mängd anilinfärger.[1]
Framställning
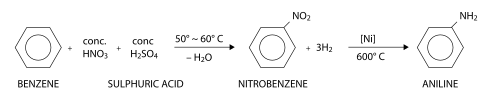
Anilin framställs huvudsakligen av bensen (C6H6) i en tvåstegsprocess där bensen först nitreras till nitrobensen (C6H5NO2) av salpetersyra (HNO3) med svavelsyra (H2SO4) som katalysator. Därefter hydrogeneras nitrobensen med vätgas till anilin med nickel eller tenn som katalysator.
Användning
Färgämnen

Anilin och dess derivat är vanliga färgämnen. Ren anilin är färglös, men vid kontakt med syror, baser, luft eller andra oxidationsmedel oxiderar den, varvid färgen framträder. Varianter, som kan bildas är 1,2-bensokinon (röd), azobensen (brandgul), 1,4-bensokinon (gul) och kloranil (gröngul).
Den färg som mest förknippas med anilin är den kraftigt violetta färgen av mauvein.
Läkemedel
Anilin används också för att framställa olika läkemedel, framför allt paracetamol.
Diverse egenskaper
- Flampunkt 70° C
- Självantändning vid 615° C
- Brytningsindex 1,5863 vid 20° C
- Permittivitet 6,89 vid 20° C
- Ytspänning
| Ytspänning (dyn/cm) | Temperatur (° C) |
|---|---|
| 44,0 | 10 |
| 42,9 | 20 |
| 24,4 | 180 |
| Viskositet (mPa·s) | Temperatur (° C) |
|---|---|
| 6,023 | 12 |
| 4,467 | 20 |
| 2,92 | 22 |
| 1,555 | 60 |

