Reguła Hückla
Reguła Hückla (reguła 4n+2) − prosta metoda pozwalająca na sprawdzenie, czy płaski pierścień związku chemicznego jest aromatyczny. Reguła ta wynika z analiz kwantowo-mechanicznych zjawiska aromatyczności wykonanych przez Ericha Hückla w 1931 r.
Reguła ta głosi:
- Związek jest prawdopodobnie aromatyczny, gdy w układzie wiązań wielokrotnych tworzących układ cykliczny tego związku występuje 4n+2 elektronów zlokalizowanych na wiązaniach π, gdzie n = dowolna liczba naturalna.
Reguła ta w praktyce jest sprawdzona dla n = od 0 do 6, przy czym zawodzi ona dla związków, w których występują więcej niż 3 sprzężone pierścienie. Np. piren i koronen są związkami aromatycznymi, mimo że nie spełniają reguły Hückla[1]. Podobnie jest też z fulerenami.
Dokładniejszym sposobem ustalania aromatyczności związków organicznych jest metoda Pariser-Parr-Pople, która jednak nie daje się sprowadzić do prostej formuły obliczeniowej.
Przykłady związków aromatycznych spełniających regułę Hückla

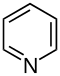
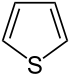
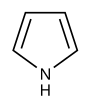
- związki zawierające heteroatomy
Przykładowe jony spełniające regułę Hückla

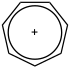
- związki jonowe
- karboaniony
- Karboaniony to rodzaj jonów, które powstają przez oderwanie atomu wodoru od atomu węgla z pozostawieniem wolnej pary elektronowej na atomie węgla. W niektórych układach cyklicznych para ta jest włączana do układu wiązań π na skutek czego jon uzyskuje cechy aromatyczności. Przykładem takiego anionu jest cyklopentadienyl.
- karbokationy
- Przykładem karbokationu spełniającego regułę Hückla jest kation cykloheptatrienylowy.
Przypisy
- ↑ Roberts, John D., Streitwieser, Andrew, Regan, Clare M.. Small-Ring Compounds. X. Molecular Orbital Calculations of Properties of Some Small-Ring Hydrocarbons and Free Radicals. „Journal of the American Chemical Society”. 74 (18), s. 4579-4582, 1952. DOI: 10.1021/ja01138a038.
Encyklopedie internetowe (ogólna zasada):