Zinktrifluormethansulfonat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
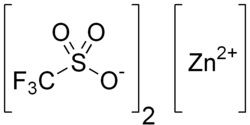
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Zinktrifluormethansulfonat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | ZnC2F6O6S2 | ||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 363,51 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Zinktrifluormethansulfonat ist eine chemische Verbindung des Zinks aus der Gruppe der Sulfonate und Salz der Trifluormethansulfonsäure.
Gewinnung und Darstellung
Zinktrifluormethansulfonat Es kann durch Reaktion von Trifluormethansulfonsäure mit Zink in Acetonitril oder mit Zinkcarbonat in Methanol hergestellt werden.[3][4]
Eigenschaften
Zinktrifluormethansulfonat ist ein weißes, kristallines Pulver, das löslich in Wasser ist.[1]
Verwendung
Zinktrifluormethansulfonat wird häufig als Lewis-Säure-Katalysator für eine Reihe von Reaktionen (zum Beispiel bei Silylierungen und der Biginelli-Reaktion[5]) verwendet.[6][7][8]
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Zinktrifluormethansulfonat, >98.0% bei TCI Europe, abgerufen am 14. September 2023.
- ↑ a b c Peter Ham: Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons, Ltd, Chichester 2001, ISBN 978-0-471-93623-7, Zinc Trifluoromethanesulfonate, doi:10.1002/047084289x.rz023.
- ↑ Jean Lombard, Sophie Romain, Stéphane Dumas, Jérôme Chauvin, Marie‐Noëlle Collomb, Denis Daveloose, Alain Deronzier, Jean‐Claude Leprêtre: Tetranuclear Polypyridyl Complexes of Ru II and Fe II : Synthesis, Electrochemical, Photophysical and Photochemical Behaviour. In: European Journal of Inorganic Chemistry. Band 2005, Nr. 16, 2005, S. 3320–3330, doi:10.1002/ejic.200500106.
- ↑ E.J. Corey, Katsuichi Shimoji: Magnesium and zinc-catalyzed thioketalization. In: Tetrahedron Letters. Band 24, Nr. 2, 1983, S. 169–172, doi:10.1016/S0040-4039(00)81357-X.
- ↑ X. u. Hui, Wang Yan-Guang: A Rapid and Efficient Biginelli Reaction Catalyzed by Zinc Triflate. In: Chinese Journal of Chemistry. 21, 2003, S. 327, doi:10.1002/cjoc.20030210321.
- ↑ Huiling Jiang, Shizheng Zhu: Silylation of 1-alkynes with chlorosilanes promoted by Zn(OTf)2: an efficient way to the preparation of alkynylsilanes. In: Tetrahedron Letters. Band 46, Nr. 3, 2005, S. 517–519, doi:10.1016/j.tetlet.2004.10.175.
- ↑ Ronaldo Aloise Pilli, Luis Gustavo Robello: Zinc Triflate as Lewis Acid in Nucleophilic Addition to Cyclic N-Acyliminium Ions. In: ChemInform. Band 37, Nr. 4, 2006, doi:10.1002/chin.200604033.
- ↑ Tse-Lok Ho: Fiesers' Reagents for Organic Synthesis, Volume 28. Wiley, 2016, ISBN 978-1-118-94281-9, S. 567 (eingeschränkte Vorschau in der Google-Buchsuche).



