Diamant
Für das Unternehmen bzw. die Marke Diamant siehe: Diamant Fahrradwerke AG.
| Diamant | |
 | |
| Chemismus | C |
| Kristallsystem | kubisch fcc |
| Kristallklasse | __ |
| Farbe | farblos, alle Farben möglich durch Verunreinigungen oder Gitterdefekte: gelblich, braun, rot, pink, grün, gelb, blau, schwarz usw. |
| Strichfarbe | weiß |
| Härte | 10 |
| Dichte | 3,52 +- 0,01 g/cm3 |
| Glanz | Diamantglanz |
| Opazität | transparent |
| Bruch | muschelig bis splittrig |
| Spaltbarkeit | vollkommen (111) |
| Habitus | gedrungen |
| häufige Kristallflächen | __ |
| Zwillingsbildung | __ |
| Kristalloptik | |
| Brechzahl | 2,417 bei = 590 nm |
| Doppelbrechung | keine; häufig anomal |
| optische Orientierung | __ |
| Winkel/Dispersion der optischen Achsen |
2vz 0.025 |
| weitere Eigenschaften | |
| chemisches Verhalten | chemisch inert gegenüber fast allen Chemikalien außer bei hohen Temperaturen Wasserstoff, Sauerstoff, Fluor; leicht löslich in Metallschmelzen kohlenstofflöslicher Metalle wie Eisen, Nickel, Kobalt, Platin, Palladium, Chrom, zum Teil unter Carbidbildung. |
| ähnliche Minerale | __ |
| Radioaktivität | in der Regel nicht radioaktiv, durch Bestrahlung oder enthaltene Verunreinigungen radioaktiv |
| Magnetismus | nicht magnetisch |
| besondere Kennzeichen | höchster Schmelzpunkt (3820 Kelvin), Wärmeleitfähigkeit fünfmal besser als Silber, elektrische Leitfähigkeit: theoretisch idealer Isolator, praktisch durch Verunreinigungen variabel, Halbleiter bis nahezu metallische Leitfähigkeit. |
Diamant (von griechisch diaphainein: durchscheinen und adamantos: das Unbezwingbare) ist neben Graphit und Fulleren eine der drei Modifikationen des Kohlenstoffs und mit einer Mohshärte von 10 das härteste natürlich vorkommende Mineral. Seine Schleifhärte ist gar 140 mal so groß wie die des Korund. Allerdings ist die Härte des Diamanten auf seinen einzelnen Kristallflächen unterschiedlich, wodurch es erst möglich wird Diamant mit Diamant zu schleifen, da in dem dazu verwendeten Diamant-Pulver jeder Härtegrad vorkommt. Diamant ist bei Raumtemperatur metastabil, die Aktivierungsenergie für den Phasenübergang in die stabile Modifikation (Graphit) ist jedoch so hoch, dass eine Umwandlung in Graphit bei Raumtemperatur praktisch nicht stattfindet. Diamant besitzt ein kubisches Kristallsystem und ist in reinem Zustand transparent, oft aber durch Verunreinigungen in den verschiedensten Farben gefärbt; die Strichfarbe ist weiß.
Die Masse einzelner Diamanten wird traditionell in Karat angegeben, einer Einheit, die 0,200 Gramm entspricht.
Neben dem eigentlichen, kubisch kristallisierenden Diamant gibt es auch eine sehr seltene hexagonale Kohlenstoff-Variante, welche als hexagonaler Diamant oder Lonsdaleit bezeichnet wird.
Aufbau und chemisches Verhalten
Exakt betrachtet ist Diamant kein reiner Kohlenstoff. Wenn auch der innere Aufbau theoretisch aus reinem Kohlenstoff besteht, so sind die freien Atombindungen an den Grenzflächen des Kristalls mit (je nachdem, was gerade "greifbar" war) Sauerstoff oder Wasserstoff gesättigt.
Im Diamant sind die Kohlenstoffatome tetraedrisch gebunden, das bedeutet, jedes Atom hat vier symmetrisch ausgerichtete Bindungen zu seinen nächsten Nachbarn. Die große Härte resultiert aus der sehr hohen Bindungsenergie der vollständig in sp3-Hybridisierung vorliegenden chemischen Bindungen.
Diamant verglüht in reinem Sauerstoff bei ca. 720 °C, in Luft bei über 800 °C zu Kohlendioxid. Mit Wasserstoff reagiert Diamant bei hohen Temperaturen zu Kohlenwasserstoffen. Diamant ist löslich in Metallschmelzen kohlenstofflöslicher Metalle und deren Legierungen, wie Eisen, Nickel, Kobalt, Chrom, Titan, Platin, Palladium und ähnlichen. Aufgrund der sehr kleinen reaktiven Oberfläche ist die Umsetzungsgeschwindigkeit auch entsprechend klein. Durch das Bestrahlen mit Neutronen bestimmter Energie läßt sich Diamant "härten". Diese Härtesteigerung des Diamanten beruht auf durch die Neutronenstrahlung bewirkten Gitterversetzungen. Diamant läßt sich aber durch Neutronenbestrahlung "aktivieren", wodurch radioaktiver Kohlenstoff C14 entsteht. Hierin liegen auch die Grenzen des Verfahrens.
Entstehung und Vorkommen

Das Muttergestein des Diamants ist der Kimberlit. Innerhalb dieses Gesteins wandelt sich der Kohlenstoff in Tiefen von oft mehr als 150 Kilometer unter hohem Druck und bei Temperaturen von bis zu 3000 °C zu Diamant um. Dieser kommt sehr schnell durch die so genannten Pipes, vulkanische Eruptivschlote, an die Erdoberfläche und kann so der Phasenumwandlung zu Graphit entgehen. Von dort können die Kristalle durch natürliche Verwitterungsprozesse, bei denen sie aufgrund ihrer Härte intakt bleiben, abtransportiert werden und reichern sich dann meist in Sedimentgesteinen an, die heute eine der Hauptquellen des Minerals darstellen.
Gewonnen werden sie zudem in den Vulkanschloten erloschener Vulkane, die senkrecht nach unten abgebaut werden. Das Muttergestein wird dabei zermahlen, um die Diamanten zu gewinnen. Im Süden Afrikas liegen Diamanten auch am Grund der Wüste, so dass der Sand bis zum gewachsenen Fels abgetragen und gewaschen werden muss.
Die größten Diamantenvorkommen befinden sich in Afrika, insbesondere in Südafrika, Namibia, Botswana, der Demokratischen Republik Kongo und Sierra Leone, in Australien und in Russland. Es wurden aber auf allen Kontinenten Diamanten gefunden. In Europa gibt es bei Archangelsk ein Vorkommen. Die Weltproduktion an Naturdiamant liegt heute bei etwa zwanzig Tonnen pro Jahr und deckt bei weitem nicht mehr den Bedarf der Industrie. Etwa 80 Prozent des Bedarfs können die Naturdiamanten nicht decken. Daher decken in steigendem Maße synthetisch erzeugte Diamanten, deren Eigenschaften wie Zähigkeit, Kristallhabitus, Leitfähigkeit und Reinheit genau bestimmt werden können, diese Lücke.
Mikrodiamanten entstehen vor allem bei Meteoriteneinschlägen: Bei den dabei auftretenden hohen Temperaturen und Drücken wird irdischer Kohlenstoff so stark komprimiert, dass sich kleine Diamantkristalle und auch Lonsdaleiten bilden, die sich aus der Explosionswolke ablagern und noch heute in der Umgebung von Meteoritenkratern wie dem Barringer-Krater nachgewiesen werden können.
Mikrodiamanten kommen auch in Fundstücken von Eisenmeteoriten und ureilitischen Achondriten vor, wo sie vermutlich durch Schockereignisse aus Graphit gebildet wurden. Winzige Diamanten, wegen ihrer typischen Größe von nur einigen Nanometern oft Nanodiamanten genannt, kommen zudem in Form von präsolaren Mineralen in primitiven Meteoriten vor.
Synthetischer Diamant
Seit 1955 ist es mit Hilfe des so genannten Hochdruck-Hochtemperatur-Verfahrens (HPHT - englisch: high-pressure high-temperature) möglich, künstliche Diamanten herzustellen. Bei diesem Verfahren wird Graphit in einer hydraulischen Presse bei Drücken von bis zu 6 Gigapascal und Temperaturen von über 1500 °C zusammengepresst. Unter diesen Bedingungen ist Diamant die thermodynamisch stabilere Form von Kohlenstoff, so dass sich der Graphit zu Diamant umwandelt. Dieser Umwandlungsprozess kann unter Beigabe eines Katalysators beschleunigt werden. Analog zum Diamant lässt sich aus der hexagonalen Modifikation des Bornitrids ebenfalls unter Verwendung der Hochdruck-Hochtemperatur-Synthese kubisches Bornitrid (CBN) herstellen. CBN erreicht allerdings nicht ganz die Härte von Diamant, ist allerdings zum Beispiel bei hohen Temperaturen gegen Sauerstoff beständig.
Parallel dazu wurde die Schockwellendiamantsynthese unter Zuhilfenahme höchster Drücke, wie sie bei Explosionen auftreten, entwickelt. Dieser kommerziell erfolgreiche Weg liefert Diamantpulver in verschiedenen Feinheiten.
Eine Alternativmöglichkeit zur Herstellung von künstlichem Diamant ist die Beschichtung von Substraten mit Hilfe der chemischen Gasphasenabscheidung (CVD - engl.: chemical vapour deposition). Dabei wird in einer Vakuumkammer eine einige Mikrometer dicke Diamantschicht auf den Substraten, zum Beispiel Hartmetallwerkzeugen, abgeschieden. Ausgangsstoff dabei ist ein Gasgemisch aus Methan und Wasserstoff, wobei ersteres als Kohlenstoffquelle dient.
Gemäß der Ostwaldschen Stufenregel sollte sich hauptsächlich metastabiler Diamat abscheiden; nach der Ostwald-Volmer-Regel bildet sich wegen seiner geringeren Dichte vorwiegend Graphit. Mit atomarem Wasserstoff gelingt es, Graphit selektiv zu zersetzen und die Bildung von Diamant zu begünstigen. Atomarer Wasserstoff (H) entsteht in einem thermisch oder elektrisch aufgeheizten Plasma aus molekularem Wasserstoff-Gas (H2).
Die Substrattemperatur muß unterhalb von 1000°C liegen, um die Umwandlung in das stabile Graphit zu unterbinden. Es lassen sich dann Wachstumsraten von mehreren Mikrometern pro Stunde erreichen.
Als weitere Entwicklung können mit Hilfe der Technik der Plasmabeschichtung nur wenige Mikrometer dünne Schichten aus so genanntem diamantartigen Kohlenstoff (DLC: diamond-like carbon) hergestellt werden. Diese Schichten vereinigen gleichzeitig die extreme Härte von Diamant und die sehr guten Gleitreibungseigenschaften von Graphit. In ihnen liegt, je nach Beschichtungsparametern, eine Mischung von sp2- und sp3-hybridisierten Kohlenstoffatomen vor.
Verwendung
Die prestigeträchtigste Anwendung finden Diamanten als hochwertige Schmucksteine. Eine höhere wirtschaftliche Bedeutung haben sie aber heute durch ihre industrielle Verwendung in der Produktion von Bohr-, Schneid-, Schleif-, Polierwerkzeugen, wobei man sich ihre große Härte, Verschleißfestigkeit und ihr Wärmeleitvermögen zunutze macht. Es ist in vielen Bereichen ausgesprochen wirtschaftlich Diamantwerkzeuge einzusetzen, wodurch Ausfallkosten und Umrüstzeiten zum Beispiel für Werkzeuge minimiert werden können. Die geforderte Oberflächenqualität läßt sich oft mit Hilfe von Diamantwerkzeugen ohne zusätzliche Bearbeitung in einem Arbeitsschritt erreichen.
Dünne Schichten aus diamantartigem Kohlenstoff dienen in großtechnischem Maßstab als Verschleißschutz. Diamantbesetzte Skalpelle könnten zum Beispiel in der Medizin zum Einsatz kommen. An mit elektrisch leitfähigem diamantbeschichteten Elektroden lassen sich chemische Reaktionen mit sehr reaktiven Radikalen realisieren. Großtechnisch kommt hier die Abwasserbehandung und -reinigung ins Blickfeld.
Durch Zusatz von Bor, Phosphor oder Stickstoff kann Diamant leitfähig gemacht werden und als Halbleiter oder sogar als Supraleiter fungieren.
Diamanten als Schmuckstein
Ein Diamant hat eine sehr hohe Lichtbrechung und einen starken Glanz, gepaart mit einer auffallenden Dispersion, weshalb er traditionell als Edelstein geschliffen wird. Erst durch die Erfindung moderner Schliffe im 20. Jahrhundert, durch die das Feuer eines Diamanten erst richtig zur Geltung kommt, wurde sein wahrer Wert offenbar. Es beruht auf zahllosen inneren Lichtreflexionen, die durch den sorgfältigen Schliff der einzelnen Facetten hervorgerufen werden, welche in speziell gewählten Winkelverhältnissen zueinander stehen müssen. Mittlerweile werden Schliffe und deren Wirkung auf Rechnern simuliert und die Steine auf Automaten geschliffen, um über eine exakte Ausführung optimale Ergebnisse zu erreichen. Nur ein Viertel aller Diamanten ist qualitativ überhaupt als Schmuckstein geeignet. Davon wiederum erfüllt nur ein kleiner Bruchteil die Kriterien, die heute an Schmucksteine gestellt werden: ausreichende Größe, geeignete Form, hohe Reinheit, und je nach Wunsch Farbigkeit oder Farblosigkeit.
Diamanten werden seit den 1980er Jahren unter anderem mit Lasern bearbeitet, um dunkle Verunreinigungen zu entfernen und Steine zu kennzeichnen. Die Eigenfarbe des Diamant lässt sich nicht so einfach wie bei anderen Schmucksteinen beeinflussen. Unansehnliche Steine gibt man zur Farbveränderung seit den 1960er Jahren in Kernreaktoren zur Bestrahlung. Das Resultat sind dauerhafte Farbveränderungen: Schmutzig-graue und gelbliche Steine erhalten ein leuchtendes Blau oder Grün. Daran kann sich noch eine Wärmebehandlung anschließen, wobei die durch Strahlung erzeugten Kristallveränderungen zum Teil wieder "ausheilen" und als weitere Farbveränderung sichtbar werden. Die Resultate sind nicht immer eindeutig vorhersehbar.
Diamantbestimmung

Kriterien zur Erkennung eines Diamanten sind seine Dichte, Härte, Wärmeleitfähigkeit, Glanz, Lichtstreuung oder Dispersion, Lichtbrechung oder Refraktion sowie Art und Ausbildung vorhandener Einschlüsse.
Ein weiteres wichtiges Unterscheidungsinstrument zwischen naturfarbenen und künstlich gefärbten Diamanten liegt in der Absorptions-Spektroskopie. Diamanten kommen in allen Farben und Schattierungen vor, doch sind es nur die gelben, braunen und grünen Diamanten, die ein Linienspektrum erzeugen. Die Farben und damit auch die Absorptionslinien beruhen auf Stickstoffbeigaben im Kohlenstoffgitter des natürlichen Diamanten.
Brillanten
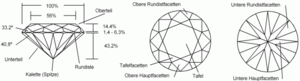
Eine besonders charakteristische - und für Diamanten die mit Abstand häufigste - Schliffform ist der Brillantschliff. Nur derartig geschliffene Diamanten dürfen als Brillanten bezeichnet werden. Zusätzliche Angaben wie echt oder ähnliche sind dabei nicht erlaubt, da irreführend. Zwar ist es möglich - und auch nicht unüblich - andere Edelsteine oder Imitate im Brillantschliff zu verarbeiten, diese müssen dann aber eindeutig bezeichnet sein, zum Beispiel als Zirkonia in Brillantschliff.
Merkmale des modernen Brillantschliffs, auch Vollbrillant genannt, sind eine kreisrunde Rundiste, mindestens 32 Facetten plus Tafel im Oberteil sowie mindestens 24 Facetten plus gegebenenfalls eine Kalette im Unterteil. Er wurde um 1910 aus dem so genannten Altschliff des vorhergehenden Jahrhunderts entwickelt. Es gibt heute unterschiedliche Varianten:
- Der Tolkowsky-Brillant von 1919 hat eine sehr gute Lichtausbeute und gilt in den USA als Grundlage der Schliffgraduierung.
- Der Ideal-Brillant, 1926 von Johnson und Rösch eingeführt, gilt im Gegensatz zu seinem Namen durchaus nicht als ideal, da seine Proportionen zu unförmig wirken.
- Der Parker-Brillant von 1951 hat eine gute Lichtausbeute, aber wegen eines recht flachen Oberteils eine geringe Dispersion, was zu einem mangelhaften Farbenspiel führt.
- Der Skandinavischer Standard-Brillant von 1968 ist wie der Name vermuten lässt in Skandinavien die Grundlage zur Graduierung.
- Der Feinschliff-Brillant von 1939 wurde von Eppler entwickelt und ist in Deutschland Grundlage der Graduierung.
Aufgrund der weitgehend feststehenden Proportionen beim Brillanten, ist es möglich anhand des Durchmessers das ungefähre Karat-Gewicht zu ermitteln.
| Durchmesser | Karat |
| 1,1 mm | 0,01 ct |
| 2,0 mm | 0,03 ct |
| 3,0 mm | 0,10 ct |
| 5,1 mm | 0,50 ct |
| 6,3 mm | 1,00 ct |
| 8,3 mm | 2,00 ct |
| 11,2 mm | 5,00 ct |
Die Entwicklung des Brillantschliffs

Der Diamant findet seit mindestens 2000 Jahren schon als Schmuckstein Verwendung, doch eine gezielte Bearbeitung setzte erst im 14. Jahrhundert ein. Zunächst aber wurden hier nur zur Erhöhung des optischen Effektes die natürlichen Kristallfächen poliert. Dieser - noch weitgehend in seiner natürlichen Form belassene - erste Diamantschliff wurde, seiner Charakteristik entsprechend, Spitzstein genannt.
Durch Abspalten oder Abschleifen der Oktaederspitzen erzeugte man bald eine zusätzliche große Fläche auf der Oberseite (Tafel) und eine kleine auf der Unterseite (Kalette) was zum so genannten Dickstein oder Tafelstein führte.
Seite Ende des 15. Jahrhunderts legte man, dank der Entwicklung der Schleifscheibe, immer mehr zusätzliche Facetten an. Um 1650 wurde - der Überlieferung nach auf Anregung des französischen Kardinals Mazarin - erstmals ein Stein mit 34 Flächen (32 Facetten plus Tafel und Kalette), sowie gerundetem, wenn auch noch nicht kreisrundem, Grundriss (Rundiste) entwickelt. Diese, Zweifaches Gut oder auch Mazarin-Schliff genannte Form, erhielt Ende des 17. Jahrhunderts durch den venezianischen Edelsteinschleifer Peruzzi seine Steigerung im so genannten Dreifachen Gut oder Peruzzi-Schliff. Dieser wies bereits alle Facetten und auch ähnliche Proportionen des späteren Brillant-Schliffes auf. Aber auch beim Altschliff, dem unmittelbaren Vorläufer des modernen Brillanten, ist der kreisrunde Körper noch nicht konsequent umgesetzt. Dies geschah erst zu Beginn des 20. Jahrhunderts.
Da der Diamant, gerade in einer schmuckwürdigen Qualität, ein sehr teurer, weil seltener und unter großem Aufwand zu gewinnender Rohstoff ist, war und ist man natürlich stets bestrebt beim Schleifen möglichst effizient zu arbeiten. Dies bedeutet, dass man versucht, unter möglichst geringem Materialverlust einen möglichst großen optischen, und somit wertsteigernden, Effekt zu erzielen.
Fancy Diamonds
Der Name Fancy Diamonds (englisch fancy "schick"), auch kurz Fancys genannt, bezeichnet farbige Diamanten. Zwar sind die meisten Diamanten farbig, viele sind jedoch unattraktiv; so kann die Eigenfarbe des Diamanten von allen Tönungen im Bereich Grau, Gelb, Grün, Braun dominiert werden; gelegentlich wechselt sie auch innerhalb eines Steines. Reine intensive Farben sind selten und wertvoll, entsprechend bessere Preise werden dafür bezahlt, die zum Teil beträchtlich über dem Standard für farblose Diamanten liegen können. Statistisch gesehen ist bei 100.000 Diamanten durchschnittlich nur ein "Fancy-Diamant" dabei. Gelb- und Brauntöne, die mehr als 80 Prozent aller farbigen Diamanten ausmachen, sind im engeren Sinne keine Fancys. Kanariengelb oder Cognacgoldbraun sind hingegen Fancy-Farben.
Die Farbbezeichnungen werden zu Verkaufszwecken gewählt: Goldorange, Lemon, Schoko, Noir/Black, Electric-Blue. Die erste große Fancy-Quelle wurde 1867 in Südafrika gefunden. Seit den 1980ern ist die Argyle Mine in Australien die wichtigste Fundstätte für pinkfarbene bis rote Fancy Diamanten.
Man unterscheidet sieben Fancy-Farben, neben denen noch viele weitere Zwischenfarben wie zum Beispiel Gold, Grau oder Gelbgrün existieren. Für die Färbung ist je ein anderer Stoff verantwortlich:
- Kanariengelb: Für die Gelbtöne ist Stickstoff verantwortlich. Je größer der Stickstoffgehalt, desto intensiver der Gelb- oder auch Grünton. Der berühmteste und wahrscheinlich größte gelbe Diamant ist der Tiffany von 128,51 Karat, sein Rohgewicht betrug 287,42 Karat. Gelb ist nach weiß und zusammen mit braun die häufigste Farbe von Diamanten.
- Braun: Für die Brauntöne sind Kristallverunreinigungen verantwortlich. Der größte braune geschliffene Diamant ist der Earth Star mit 111,6 Karat. Der größte je gefundene braune Diamant ist wahrscheinlich der Lesotho mit 601 Karat.
- Blau: Das Element Bor ist für die blaue Färbung von Diamanten verantwortlich. Der größte und berühmteste blaue Diamant ist der angeblich verfluchte Hope-Diamant, welcher ungeschliffen 112,5 Karat wog und in geschliffenem Zustand heute 45,52 Karat wiegt. Blaue Diamanten sind sehr selten, doch häufiger als grün oder rot.
- Grün: Der bekannteste und vielleicht auch größte Diamant dieser Farbe ist der Dresden-Diamant mit einem Gewicht von 41,0 Karat (ungeschliffen 119,5 Karat). Grüne Diamanten sind sehr selten.
- Rot: Vermutlich sind Kristalldefekte verantwortlich für diese Färbung. Der größte je gefundene rote Diamant ist der australische Red Diamond mit einem Rohgewicht von 35 Karat. Der größte geschliffene Diamant ist der ebenfalls australische Red Shield mit 5,11 Karat. Reine rote Diamanten sind die seltensten unter allen Diamanten. 90 Prozent der roten Diamanten stammen von der Argyle Mine in Australien. Von den purpurnen Diamanten existieren nur zehn Exemplare, wovon der größte 3 Karat wiegt. Alle kamen ebenfalls aus der Argyle Mine. Rote Diamanten sind die teuersten aller Diamanten.
- Pink oder Rosa: Oft werden pinkfarbene Diamanten zu den roten Diamanten gezählt. Auch hier sind Kristallunreinheiten für die Farbe verantwortlich. Der größte Rohdiamant ist der Daya-I-Nur mit einem Gewicht von 285 Karat, der größte geschliffene Diamant der Steinmetz Pink mit 59,6 Karat. Von den 66 größten Diamanten ist nur einer rosa gefärbt.
Reinheit
Zur Beschreibung der Reinheit werden folgende Abkürzungen und Fachbegriffe verwendet (Rangfolge):
- if (internally flawless) - lupenrein
- vvs (very, very small inclusions) - sehr, sehr kleine Einschlüsse
- vs (very small inclusions) - sehr kleine Einschlüsse
- si (small inclusions) - kleine Einschlüsse
- p1 (Piqué 1) - Einschlüsse mindern die Brillanz nicht
- p2 (Piqué 2) - Einschlüsse mindern die Brillanz nur schwach
- p3 (Piqué 3) - Einschlüsse mindern die Brillanz deutlich
Große und berühmte Diamanten
In der folgenden Tabelle sind einige besonders berühmte Diamanten zusammen mit ihrem Fundgewicht sowie Fundort und -jahr aufgeführt:
| Name | Rohgewicht | Fundjahr | Fundland | Bemerkung |
|---|---|---|---|---|
| Cullinan | 3106 Karat | 1905 | Südafrika | Wurde in 105 Steine aufgespalten. |
| Excelsior | 995,20 Karat | 1893 | Südafrika | Wurde in 22 Steine aufgespalten. |
| Star of Sierra Leone | 968,90 Karat | 1972 | Sierra Leone | Wurde in 17 Steine aufgespalten. |
| Incomparable | 797,5 Karat | 1650 | Indien | bläulicher Diamant; gilt seit 1739 als verschwunden. |
| Präsident Vargas | 726,8 Karat | 1938 | Brasilien | |
| Jonker | 726 Karat | 1934 | Südafrika | |
| Koh-i-Noor | 186 Karat | ca. 3000 v. Chr. | evt. Indien | ältester bekannter Diamant; heute im Tower of London |
| Florentiner | 137,27 Karat | unbekannt | unbekannt | gelber Diamant; Verbleib nach dem 1. Weltkrieg unbekannt |
| Regent od. Pitt | 136,75 Karat | um 1700 | Indien | heute im Louvre |
| Hope | 112,5 Karat | unbekannt | Indien | blauer Diamant; 1642 erstmals aufgetaucht, heute als Dauerleihgabe in der Smithsonian Institution in Washington zu sehen |
| Schah | 86 Karat | unbekannt | unbekannt | mit Gravur seiner drei königlichen Besitzer (einer war Schah Janan, deshalb sein Name); heute im Kreml in Moskau |
| Sancy | 55 Karat | unbekannt | Indien | |
| Dresden Diamant | 41 Karat | um 1743 | Indien | Grüne Farbe, heute im Grünen Gewölbe in Dresden |
Soziale Einflüsse
Während der Großteil der heutigen Diamanten mit modernen Mitteln von sehr wenigen international operierenden Konzernen wie der Firma De Beers abgebaut wird, kommt es durch den exorbitanten Preis, der für Diamanten gezahlt wird, vor allem in den unterentwickelten Regionen und Krisengebieten der Welt zu Grabungen unter erbärmlichen und zum Teil lebensgefährlichen Bedingungen. Selbst wenn einzelne der Arbeiter fündig werden, werden die Rohdiamanten zumeist billig an die lokalen Kriegsherren verkauft, so dass nur ein Bruchteil der Gewinne bei den eigentlichen Produzenten verbleibt.
Mit den Gewinnen aus dem Diamantenhandel werden auf dem afrikanischen Kontinent auch viele Bürgerkriege finanziert, so zum Beispiel in der Demokratischen Republik Kongo. Auch aus diesem Grunde wird heute versucht, den Handel mit diesen Blutdiamanten beziehungsweise Konfliktdiamanten zu unterbinden. Allerdings ist es praktisch nicht möglich einem Diamanten seine Herkunft anzusehen, und Zertifikate, die dies ermöglichen sollen, werden häufig gefälscht.
Geschichte
Der erste überlieferte Diamantfund stammte aus dem 4. Jahrtausend v. Chr. aus Indien. Bereits damals sagte man Diamanten magische Wirkungen nach, weshalb man sie auch als Talismane nutzte. Diamanten waren auch bei den alten Römern bekannt und wurden sehr geschätzt. Die Verwendung von Diamanten als Werkzeug beschreibt schon Plinius der Ältere in seinem Werk Naturalis historia, XXXVII 60 . Um 600 n. Chr. wurde der erste Diamant auf der indonesischen Insel Borneo gemeldet, doch obwohl Indien nun nicht mehr die einzige Quelle war, blieben die indonesischen Funde unbedeutend, da die Anzahl zu gering und der Transport zu den Handelsstädten zu weit war. Erst im 13. Jahrhundert entdeckte man, dass sich Diamanten bearbeiten lassen, was jedoch in Indien abgelehnt wurde, da die Steine so angeblich ihre magischen Kräfte verlieren könnten. Der heutige typische Brillantschliff wurde erst um 1910 entwickelt..
Im 18. Jahrhundert fingen die indischen (und auch die indonesischen) Minen an sich zu erschöpfen. Als ein Portugiese auf der Suche nach Gold in Brasilien war, entdeckte er den ersten Diamanten außerhalb Asiens. Dieser Fund verursachte einen "Diamantenrausch". Den ersten Diamanten im Muttergestein Kimberlit fand man 1869 im Südafrika Kimberley. Ein Jahr später übernahm Südafrika die Rolle des Hauptlieferanten, da auch Brasiliens Funde seltener wurden. Auf der Weltausstellung in Philadelphia 1876 wurden erstmals mit Diamanten besetzte Steinsägemaschinen einer breiten Öffentlichkeit gezeigt. 1926 entdeckte man auch an der Atlantikküste Diamanten und 1955 wurde schließlich der erste Diamant künstlich hergestellt. Den ersten Diamanten auf dem Meeresgrund fand man erst 1961. Heute ist Australien Hauptlieferant für Diamanten.
Weitere Erstfunde
- 1826 in Russland
- 1851 in Australien (erster in Australien)
- 1867 in Südafrika (erster in Afrika)
- 1901 in Venezuela
- 1906 in den USA (Bundesstaat Arkansas)
- 1906 auf dem Gebiet der heutigen Demokratischen Republik Kongo
- 1908 in Namibia
- 1912 in Angola
- 1920 an der Westküste Afrikas (Ghana)
- 1969 in China
Siehe auch: Liste von Mineralen, Diamantoide, Adamantan
Literatur
- Ulrich Schwarz: Diamant: naturgewachsener Edelstein und maßgeschneidertes Material. Chemie in unserer Zeit 34(4), S. 212 - 222 (2000), ISSN 0009-2851

