Rab-Proteine
Die Familie der Rab-Proteine („Ras-related in brain“) gehört zur Ras-Superfamilie monomerer G-Proteine (GTPasen) und ist in Eukaryoten zu großen Teilen konserviert. Bei Menschen gibt es über 60 bekannte Rab-Proteine, die jeweils eine spezifische subzelluläre Lokalisation aufweisen und eine Rolle bei der intrazellulären Vesikelsortierung zwischen den verschiedenen Kompartimenten spielen. Allgemein wird eine aktive Form, in der GTP gebunden ist und eine inaktive, GDP-haltige Form unterschieden.
Eigenschaften
Rabs sind periphere Membranproteine, die von der Vesikeloberfläche ins Cytosol ragen und über einen Prenylanker in der Membran fixiert sind. Nach der Synthese wird ein Rab-Protein zunächst durch das Rab escort protein (REP) gebunden und dem Enzym Geranylgeranyltransferase präsentiert, das für die Prenylierung von meist zwei C-terminalen Cystein-Resten sorgt. REP fungiert im Folgenden als eine Art Chaperon, das den hydrophoben Teil des Moleküls gegen das Cytosol abschirmt und zur Membran transportiert.
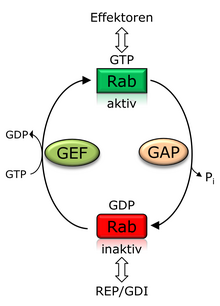
Rab-Proteine durchlaufen wie für G-Proteine üblich einen sogenannten GTPase-Zyklus. Die Aktivierung von Rab-Proteinen erfolgt durch Austausch von GDP gegen GTP mit Hilfe eines GTP-Austauschfaktors (GEF, engl. guanine nucleotide exchange factor). Der GEF sorgt dabei für die Freisetzung vom gebundenen GDP, sodass das in höherer zytosolischer Konzentration vorliegende GTP an das Rab-Protein binden kann. Die Bindung von GTP sorgt für Konformationsänderungen in den als Switch I und Switch II bezeichneten Regionen des Rab-Proteins, sodass es im Folgenden mit Effektorproteinen interagieren kann. Über die Effektorproteine wird der Vesikeltransport in der Zelle (zwischen den Organellen sowie zwischen ihnen und der Plasmamembran) über Einflussnahme auf Vesikelabschnürung, -bewegung und -fusion reguliert. Zu den Effektorproteinen gehören Enzyme, Proteine des Cytoskeletts genauso wie weitere Proteine, die an der gerichteten Membranfusion beteiligt sind. Die Inaktivierung erfolgt durch GTP-Hydrolyse, die von einem sogenannten GTPase-aktivierenden Protein (GAP) unterstützt wird. Im inaktiven Zustand kann das Rab-Protein durch den sogenannten GDP-Dissoziations-Inhibitor (GDI), der eine strukturelle Ähnlichkeit zu REP aufweist, aus der Membran extrahiert und im Zytosol löslich gehalten werden. Gekoppelt an den Wechsel zwischen GTP/GDP-Bindung ist zusätzlich ein Zyklus der Lokalisation zwischen Zytosol und Membran gekoppelt. Die Aktivierung des Rab-Proteins erfolgt im Wesentlichen an der Donormembran, sodass aktive Rab-Proteine membranlokalisiert vorliegen. Nach erfolgtem vesikulärem Transport werden die Rab-Proteine an der Akzeptormembran inaktiviert und wieder durch GDI ins Zytosol überführt, sodass sie für weitere Rekrutierungsprozesse zur Donormembran zur Verfügung stehen. Im inaktiven GDP-gebundenen Zustand liegen Rab-Proteine demnach vorwiegend zytosolisch vor.
Die mehr als 60 verschiedenen humanen Rab-Proteine sind in der Zelle spezifisch lokalisiert und regulieren zwischen bestimmten Kompartimenten den Membrantransport. Eine Auswahl an Lokalisationen und Funktionen ist in folgender Tabelle dargestellt.
| Protein | Organell (Lokalisation) | entsprechender Membrantransportweg/Funktion |
|---|---|---|
| Rab1 | Endoplasmatisches Retikulum (ER) und Golgi-Apparat | Transport vom ER zum Golgi |
| Rab2 | cis-Golgi-Netzwerk | Transport vom ER zum Golgi |
| Rab3A | synaptische Vesikel, sekretorische Granula | Exozytose, Neurotransmitter-Freisetzung |
| Rab4 | frühe Endosomen | Proteinrecycling, Transport zur Plasmamembran |
| Rab5A-C | Plasmamembran, Clathrin-umhüllte Vesikel, frühe Endosomen | Fusion früher Endosomen |
| Rab6 | mediales und trans-Golgi-Netzwerk (TGN) | Transport von Endosomen zum Golgi-Apparat, innerhalb vom Golgi und vom Golgi zum ER |
| Rab7 | späte Endosomen, Lysosomen, Melanosomen, Phagosomen | Transport von späten Endosomen zu Lysosomen |
| Rab8 | sekretorische Vesikel, Zellmembran, Zilien | Exozytose, Transport vom TGN sowie Recyclingendosomen zur Plasmamembran |
| Rab9 | späte Endosomen, TGN | Transport später Endosomen zum TGN |
| Rab27 | Melanosomen | Exozytose |
Der Mechanismus der Lokalisation der verschiedenen Rab-Proteine an ihre spezifischen Donormembranen ist noch nicht genau geklärt. Es existieren aber verschiedene Modelle:
- Ein frühes Modell (Chavrier u. a., 1991[1]) implizierte, dass die hypervariable Region der Rab-Proteine im C-terminalen Bereich eventuell für die Lokalisation verantwortlich ist. Dies wurde durch Austausch des C-Terminus von Rab5 durch den von Rab7 und eine entsprechende Lokalisationsveränderung gezeigt.
- Zudem wurde ein sogenannter GDI displacement factor (GDF) (Yip3) identifiziert. Dabei handelt es sich um ein integrales Membranprotein, das für die Freisetzung des Rab-Proteins aus dem Komplex mit GDI und folgende Integration des Rab-Proteins in die Zielmembran sorgen soll.[2]
- Ein drittes Modell sieht die GEFs als ausreichenden Faktor für die Lokalisation der Rab-Proteine.[3]
Erkrankungen
Eine Variante des Griscelli-Syndroms wird verursacht durch eine Punktmutation in dem Gen, das Rab27a kodiert. Dabei ist der Transport von Melanosomen zur Zellperipherie und die Sekretion lytischer Granula aus cytotoxischen T-Zellen gestört. Rab25 gilt als Promoter für die Tumorentwicklung.[4]
Choroideremia ist eine X-chromosomal vererbte Erkrankung, die zur Degeneration des retinalen Epithels und Blindheit führen kann. Betroffen ist dabei die REP-Isoform REP-1, das spezifisch in der Retina für die Prenylierung von Rab27a verantwortlich ist.
Eine Mutation in GDI-α, einer vor allem in Synapsen des ZNS vorkommenden Isoform, kann zu X-chromosomal vererbter geistiger Retardierung führen, da das Recycling von Rab eingeschränkt ist.
Siehe auch
Quellen
- H. Stenmark, V. M. Olkkonen: The Rab GTPase family. In: Genome biology. Band 2, Nummer 5, 2001, S. REVIEWS3007, PMID 11387043, PMC 138937 (freier Volltext) (Review).
- H. Stenmark: Rab GTPases as coordinators of vesicle traffic. In: Nat Rev Mol Cell Biol. 10(8), 2009, S. 513–525. PMID 19603039
- A. H. Hutagalung, P. J. Novick: Role of Rab GTPases in Membrane Traffic and Cell Physiology. In: Physiol Rev. 91, 2011, S. 119–149. PMID 21248164
Einzelnachweise
- ↑ P. Chavrier, J. P. Gorvel, E. Stelzer, K. Simons, J. Gruenberg, M. Zerial: Hypervariable C-terminal domain of rab proteins acts as a targeting signal. In: Nature. 1991, 353(6346), S. 769–772. PMID 1944536
- ↑ U. Sivars, D. Aivazian, S. R. Pfeffer: Yip3 catalyses the dissociation of endosomal Rab-GDI complexes. In: Nature. 2003, 425(6960), S. 856–859. PMID 14574414
- ↑ Y. W. Wu, L. K. Oesterlin, K. T. Tan, H. Waldmann, K. Alexandrov, R. S. Goody: Membrane targeting mechanism of Rab GTPases elucidated by semisynthetic protein probes. In: Nat Chem Biol. 2010, 6(7), S. 534–540. PMID 20512138.
- ↑ D Kessler, GC Gruen, D Heider, J Morgner, H Reis, KW Schmid, V Jendrossek: The action of small GTPases Rab11 and Rab25 in vesicle trafficking during cell migration. In: Cellular physiology and biochemistry : international journal of experimental cellular physiology, biochemistry, and pharmacology. 29. Jahrgang, Nr. 5–6, 2012, S. 647-56, PMID 22613965.
