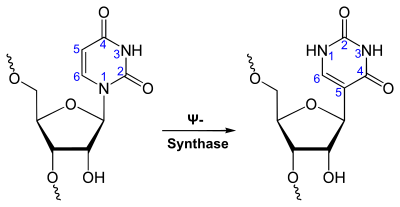Pseudouridin
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||
| Allgemeines | ||||||||||
| Name | Pseudouridin | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C9H12N2O6 | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 244,20 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Pseudouridin (abgekürzt nach dem griechischen Buchstaben Psi, Ψ) ist ein natürlich vorkommendes Nukleosid. Es besteht aus der β-D-Ribose (Zucker) und der Nukleinbase Uracil. Pseudouridin ist ein Isomer des Uridins; Ψ-Synthasen katalysieren die Umlagerung.
Geschichte
Pseudouridin (Ψ) wurde Anfang der 1950er-Jahre als erstes natürliches modifiziertes Nukleosid entdeckt[3] und zählt zu den häufigsten modifizierten Nukleosiden. Es kommt insbesondere in tRNA in der TΨC-Schleife vor.[4]

Eine tRNAAla aus S. cerevisiae. Pseudouridin ist hier mit Ψ gekennzeichnet und kommt an zwei Stellen vor.
Eigenschaften
Pseudouridin bildet mit Adenosin ein Basenpaar.
Chemisch handelt es sich um ein C-Glycosid, bei dem die β-D-Ribose mit dem C5-Atom der Base Uracil verknüpft ist. Im Uridin dagegen ist die Ribose mit dem N1-Atom des Uracils verknüpft.
Pseudouridin wird erst nach der Transkription (posttranskriptional) aus Uridin gebildet. Diese Isomerisierung katalysieren Ψ-Synthasen, was in der Literatur als Pseudouridylation bezeichnet wird.[5][6]
Verwendung in modRNA
Pseudouridin wird neben anderen natürlich vorkommenden und nur in-vitro synthetisierten modifizierten Nukleosiden zur Synthese von modRNA verwendet.[7] Im SARS-CoV-2-Impfstoff Tozinameran wurden alle Uracil-Nukleinbasen (beziehungsweise Uridine) durch das Pseudouridin-Derivat N1-Methylpseudouridin ersetzt (siehe auch Nukleosid-modifizierte mRNA).[8][9]
Siehe auch
Literatur
- M. Charette, M. W. Gray: „Pseudouridine in RNA: What, Where, How, and Why“, in: IUBMB Life, 2000, 49 (5), S. 341–351 (PMID 10902565; doi:10.1080/152165400410182).
Einzelnachweise
- ↑ W. E. Cohn: „Pseudouridine, a Carbon-Carbon Linked Ribonucleoside in Ribonucleic Acids: Isolation, Structure, and Chemical Characteristics“, in: J. Biol. Chem., 1960, 235 (5), S. 1488–1498 (PMID 13811056; PDF).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ W. E. Cohn und E. Volin: „Nucleoside-5'-Phosphates from Ribonucleic Acid“, in: Nature, 1951, 167, S. 483–484 (doi:10.1038/167483a0).
- ↑ T. Hamma und A. R. Ferré-D'Amaré: „Pseudouridine Synthases“, in: Chem. Biol., 2006, 13 (11), S. 1125–1135 (PMID 17113994).
- ↑ R. Cortese, H. O. Kammen, S. J. Spengler, B. N. Ames: „Biosynthesis of Pseudouridine in Transfer Ribonucleic Acid“, in: J. Biol. Chem., 1974, 249 (6), S. 1103–1108 (PMID 4592259; PDF).
- ↑ A. R. Ferré-D'Amaré: „RNA-Modifying Enzymes“, in: Curr Opin Struct Biol, 2003, 13 (1), S. 49–55 (PMID 12581659; doi:10.1016/S0959-440X(02)00002-7).
- ↑ Katalin Karikó, Michael Buckstein, Houping Ni, Drew Weissman: Suppression of RNA Recognition by Toll-like Receptors: The Impact of Nucleoside Modification and the Evolutionary Origin of RNA. In: Immunity. Band 23, Nr. 2, August 2005, S. 165–175, doi:10.1016/j.immuni.2005.06.008.
- ↑ European medicines Agency Assessment report on Comirnaty (Common name: COVID-19 mRNA vaccine) (nucleoside-modified) Procedure No. EMEA/H/C/005735/0000.
- ↑ Elie Dolgin: Der verschlungene Weg zum RNA-Impfstoff, Spektrum 3/2022 S. 28–37, Epub 16. Februar 2022.
Weblinks
- Eintrag zu Pseudouridine in der Human Metabolome Database (HMDB), abgerufen am 24. September 2013.
- Modification Summary von Pseudouridine in der Modomics-Datenbank, abgerufen am 14. Januar 2014.