Lebensmittelbräunung
Lebensmittelbräunung bezeichnet die braune Verfärbung von Lebensmitteln. Sie entsteht durch unterschiedliche chemische Reaktionen. Die Lebensmittelbräunung wird in enzymatische Bräunung (unter Einwirkung von Enzymen) und nichtenzymatische Bräunung (ohne Einwirkung von Enzymen) unterteilt.
Eigenschaften
Bei der Herstellung und Lagerung von Lebensmitteln ist die Bräunung von Lebensmitteln eine der wichtigsten chemischen Reaktionen.[1] Die Lebensmittelbräunung wirkt sich neben der Färbung auf den Geschmack, den Nährstoffgehalt und den Wert eines Lebensmittels aus.[2][3][4][5][6] Während viele Lebensmittelbräunungen unerwünscht sind und als Teil eines Verderbs des Lebensmittels angesehen werden, gibt es auch erwünschte Bräunungen bei der Herstellung von Lebensmitteln,[1] beispielsweise beim Backen von Brot oder beim Anbraten von Fleisch oder Kartoffeln. Bei der industriellen Herstellung von Lebensmitteln werden verschiedene Methoden zur Vermeidung einer unerwünschten Lebensmittelbräunung verwendet.[7]
Enzymatische Bräunung

Die enzymatische Bräunung entsteht durch eine Oxidation von phenolischen Stoffen in Anwesenheit von Luftsauerstoff zu Chinonen durch die Polyphenoloxidase und erfolgt insbesondere in Obst, Gemüse, Fisch und Meeresfrüchten.[1] Die Cofaktoren der Polyphenoloxidase sind Kupferionen. In Folge der Reaktionen der Polyphenoloxidase reagieren die elektrophilen Chinone mit den nukleophilen Aminogruppen.[8] Anschließend werden über nichtenzymatische Reaktionen polymere Melanoidine gebildet.[9] Die Bräunungsrate korreliert mit der Konzentration der Polyphenoloxidase im Lebensmittel.[1] Daher werden Methoden zur Minderung der Lebensmittelbräunung durch Hemmung der Polyphenoloxidase untersucht.[1] Neben der Polyphenoloxidase werden Chinone auch durch die Laccase gebildet.[10]
Nichtenzymatische Bräunung

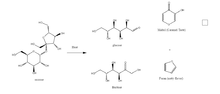
Die nichtenzymatische Bräunung bezieht sich vor allem auf die Reaktion von Amin-haltigen Stoffen (wie Aminosäuren, Peptide und Proteine) mit den Carbonylgruppen von reduzierenden Zuckern, Ascorbinsäure (Vitamin C), den Oxidationsprodukten der Ascorbinsäure oder oxidierten Fetten über die Maillard-Reaktion.[1] Bei trockenen Gartechniken wie Braten, Backen oder Frittieren wird die Bräunung beschleunigt. Dabei laufen die verschiedenen Reaktionen parallel ab.[11] Daneben entsteht eine Bräunung von Lebensmitteln über die Karamellisierungsreaktion.[1]
Hemmung der Lebensmittelbräunung
Hemmung der enzymatischen Bräunung
Säuren wie beispielsweise die Zitronensäure und Ascorbinsäure aus Zitronensaft senken den pH-Wert und entfernen die Kupferionen aus dem aktiven Zentrum der Polyphenoloxidase, beispielsweise bei Äpfeln.[12][13] Zitronensäure ist nebenbei ein Chelator und bindet Kupferionen, ebenso binden manche Proteine Kupferionen.[14] Ascorbinsäure senkt als Antioxidans die Konzentration an Sauerstoff durch Reaktion. Garen von Lebensmitteln führt zu einer Denaturierung der Proteine, einschließlich der Polyphenoloxidase, deren Enzymaktivität dadurch verloren geht. Kühlen und Tiefkühlen senken die Enzymaktivität der Polyphenoloxidase. Ein Sauerstoffentzug durch Vakuumverpackung oder Schutzgasverpackung hemmt ebenfalls die Bräunung. Die enzymatische Bräunung kann durch Hemmstoffe der Polyphenoloxidase gemindert werden.[15] Daher werden Hemmstoffe der Polyphenoloxidase und der von ihr katalysierten Reaktion untersucht, wie beispielsweise Ascorbinsäure,[12][13] Methyl-trans-Zimtsäure,[16] 2R,3R-Dihydromyricetin,[17] Omeprazol,[18] Benzylidenaceton, Benzylaceton, 4-Phenyl-2-butanol,[19] verschiedene Hydroxypyridinone,[20] Glykolsäure,[21] Salicylsäure,[22] Abscisinsäure,[23] Phytinsäure,[24] Gewürznelkenöl und das darin enthaltene Eugenol,[25] die Aminosäure Cystein,[26] das Tripeptid Glutathion (Glutaminsäure-Cystein-Glycin, Kurzschreibweise ECG),[27] Maillard-Reaktionsprodukte von Glucose oder Fructose mit Cystein oder Glutathion,[28] das Heptapeptid Isoleucin-Glutamin-Serin-Prolin-Histidin-Phenylalanin-Phenylalanin (Kurzschreibweise: IQSPHFF),[29] Propylgallat,[30] Natriummetabisulfit, Extrakte von Chilischoten, Ananas und erhitzten Küchenzwiebeln,[31] erhitzte Extrakte der Nektarine,[32] sowie Extrakt der Miesmuschel.[33]
Hemmung der nichtenzymatischen Bräunung
Die nichtenzymatische Bräunung kann durch verschiedene Methoden verlangsamt werden. Darunter fallen unter anderem die chemische Modifikation und die Entfernung von Reaktanden und Reaktionsprodukten, die Vermeidung der Oxidation durch Zugabe von Antioxidantien (beispielsweise durch Ascorbinsäure) und die Veränderung der Zusammensetzung des Lebensmittels.[34]
Literatur
- E. Dworschák: Nonenzyme browning and its effect on protein nutrition. In: Critical reviews in food science and nutrition. Band 13, Nummer 1, 1980, S. 1–40, doi:10.1080/10408398009527292, PMID 6996923.
Einzelnachweise
- ↑ a b c d e f g Marta Corzo-Martínez, Nieves Corzo, Mar Villamiel, M Dolores del Castillo: Food Biochemistry and Food Processing. Hrsg.: Benjamin K. Simpson Ph.D. Wiley-Blackwell, 2012, ISBN 978-1-118-30803-5, S. 56–83, doi:10.1002/9781118308035.ch4/summary (englisch, wiley.com).
- ↑ Thomas Richardson, John W. Finley: Chemical Changes in Food during Processing. Springer Science & Business Media, 1986, ISBN 978-0-87055-504-6, S. 123.
- ↑ Daniel Holderbaum,: Enzymatic Browning, Polyphenol Oxidase Activity, and Polyphenols in Four Apple Cultivars: Dynamics during Fruit Development. HortScience, 2010.
- ↑ M. Ümit Ünal: Properties of polyphenol oxidase from Anamur banana (Musa cavendishii). In: Food Chemistry. 100. Jahrgang, Nr. 3, S. 909–913, doi:10.1016/j.foodchem.2005.10.048.
- ↑ Vámos-Vigyázó L: Polyphenol oxidase and peroxidase in fruits and vegetables. In: Critical Reviews in Food Science and Nutrition. 15. Jahrgang, Nr. 1, S. 49–127, doi:10.1080/10408398109527312, PMID 6794984.
- ↑ Thygesen PW, Dry IB, Robinson SP: Polyphenol oxidase in potato. A multigene family that exhibits differential expression patterns. In: Plant Physiology. 109. Jahrgang, Nr. 2, Oktober 1995, S. 525–31, doi:10.1104/pp.109.2.525, PMID 7480344, PMC 157616 (freier Volltext) – (plantphysiol.org).
- ↑ A. Kaanane, T. P. Labuza: The Maillard reaction in foods. In: Progress in Clinical and Biological Research. 304. Jahrgang, 1. Januar 1989, ISSN 0361-7742, S. 301–327, PMID 2675033.
- ↑ J. J. Macheix, J. C. Sapis, A. Fleuriet: Phenolic compounds and polyphenoloxidase in relation to browning in grapes and wines. In: Critical Reviews in Food Science and Nutrition. 30. Jahrgang, Nr. 4, 1. Januar 1991, ISSN 1040-8398, S. 441–486, doi:10.1080/10408399109527552, PMID 1910524.
- ↑ J. J. Nicolas, F. C. Richard-Forget, P. M. Goupy, M. J. Amiot, S. Y. Aubert: Enzymatic browning reactions in apple and apple products. In: Critical Reviews in Food Science and Nutrition. 34. Jahrgang, Nr. 2, 1. Januar 1994, ISSN 1040-8398, S. 109–157, doi:10.1080/10408399409527653, PMID 8011143.
- ↑ John R. Whitaker: Principles of Enzymology for the Food Sciences, Second Edition,. CRC Press, 1993, ISBN 978-0-8247-9148-3, S. 543.
- ↑ R. Zamora, F. J. Hidalgo: Coordinate contribution of lipid oxidation and Maillard reaction to the nonenzymatic food browning. In: Critical reviews in food science and nutrition. Band 45, Nummer 1, 2005, S. 49–59, doi:10.1080/10408690590900117, PMID 15730188.
- ↑ a b N. M. el-Shimi: Control of enzymatic browning in apple slices by using ascorbic acid under different conditions. In: Plant Foods for Human Nutrition (Dordrecht, Netherlands). 43. Jahrgang, Nr. 1, 1. Januar 1993, ISSN 0921-9668, S. 71–76, PMID 8464847.
- ↑ a b FRANCESCO PIZZOCARO, DANILA TORREGGIANI, GIANLUCA GILARDI: INHIBITION of APPLE POLYPHENOLOXIDASE (PPO) BY ASCORBIC ACID, CITRIC ACID and SODIUM CHLORIDE. In: Journal of Food Processing and Preservation. 17, 1993, S. 21, doi:10.1111/j.1745-4549.1993.tb00223.x.
- ↑ Nilesh Prakash Nirmal, Soottawat Benjakul, Mehraj Ahmad, Yasir Ali Arafat, Pharkphoom Panichayupakaranant: Undesirable Enzymatic Browning in Crustaceans: Causative Effects and Its Inhibition by Phenolic Compounds. In: Critical Reviews in Food Science and Nutrition. 55. Jahrgang, Nr. 14, 1. Januar 2015, ISSN 1549-7852, S. 1992–2003, doi:10.1080/10408398.2012.755148, PMID 25584522.
- ↑ T. S. Chang: An updated review of tyrosinase inhibitors. In: International Journal of Molecular Sciences. Band 10, Nummer 6, Mai 2009, S. 2440–2475, doi:10.3390/ijms10062440, PMID 19582213, PMC 2705500 (freier Volltext).
- ↑ Q. S. Huang, Y. J. Zhu, H. L. Li, J. X. Zhuang, C. L. Zhang, J. J. Zhou, W. G. Li, Q. X. Chen: Inhibitory effects of methyl trans-cinnamate on mushroom tyrosinase and its antimicrobial activities. In: Journal of agricultural and food chemistry. Band 57, Nummer 6, März 2009, S. 2565–2569, doi:10.1021/jf8036227, PMID 19231901.
- ↑ X. Liang, Y. P. Wu, J. H. Qiu, K. Zhong, H. Gao: A potent antibrowning agent from pine needles of Cedrus deodara: 2R,3R-dihydromyricetin. In: Journal of food science. Band 79, Nummer 9, September 2014, S. C1643–C1648, doi:10.1111/1750-3841.12583, PMID 25163933.
- ↑ M. Z. Lin, W. M. Chai, C. Ou-Yang, Q. Huang, X. H. Xu, Y. Y. Peng: Antityrosinase mechanism of omeprazole and its application on the preservation of fresh-cut Fuji apple. In: International journal of biological macromolecules. Band 117, Oktober 2018, S. 538–545, doi:10.1016/j.ijbiomac.2018.05.172, PMID 29803745.
- ↑ X. Liu, Y. L. Jia, J. W. Chen, G. Liang, H. Y. Guo, Y. H. Hu, Y. Shi, H. T. Zhou, Q. X. Chen: Inhibition effects of benzylideneacetone, benzylacetone, and 4-phenyl-2-butanol on the activity of mushroom tyrosinase. In: Journal of bioscience and bioengineering. Band 119, Nummer 3, März 2015, S. 275–279, doi:10.1016/j.jbiosc.2014.08.014, PMID 25441446.
- ↑ L. L. Shao, X. L. Wang, K. Chen, X. W. Dong, L. M. Kong, D. Y. Zhao, R. C. Hider, T. Zhou: Novel hydroxypyridinone derivatives containing an oxime ether moiety: Synthesis, inhibition on mushroom tyrosinase and application in anti-browning of fresh-cut apples. In: Food chemistry. Band 242, März 2018, S. 174–181, doi:10.1016/j.foodchem.2017.09.054, PMID 29037675.
- ↑ D. Ma, Z. C. Tu, H. Wang, L. Zhang, N. He, D. J. McClements: Mechanism and kinetics of tyrosinase inhibition by glycolic acid: a study using conventional spectroscopy methods and hydrogen/deuterium exchange coupling with mass spectrometry. In: Food & function. Band 8, Nummer 1, Januar 2017, S. 122–131, doi:10.1039/c6fo01384h, PMID 27929190.
- ↑ D. Zhou, L. Li, Y. Wu, J. Fan, J. Ouyang: Salicylic acid inhibits enzymatic browning of fresh-cut Chinese chestnut (Castanea mollissima) by competitively inhibiting polyphenol oxidase. In: Food chemistry. Band 171, März 2015, S. 19–25, doi:10.1016/j.foodchem.2014.08.115, PMID 25308637.
- ↑ Q. Zhang, Y. Liu, C. He, S. Zhu: Postharvest Exogenous Application of Abscisic Acid Reduces Internal Browning in Pineapple. In: Journal of agricultural and food chemistry. Band 63, Nummer 22, Juni 2015, S. 5313–5320, doi:10.1021/jf506279x, PMID 26007196.
- ↑ Y. Du, S. Dou, S. Wu: Efficacy of phytic acid as an inhibitor of enzymatic and non-enzymatic browning in apple juice. In: Food chemistry. Band 135, Nummer 2, November 2012, S. 580–582, doi:10.1016/j.foodchem.2012.04.131, PMID 22868131.
- ↑ X. Chen, L. Ren, M. Li, J. Qian, J. Fan, B. Du: Effects of clove essential oil and eugenol on quality and browning control of fresh-cut lettuce. In: Food chemistry. Band 214, Januar 2017, S. 432–439, doi:10.1016/j.foodchem.2016.07.101, PMID 27507495.
- ↑ X. Zhou, Y. Xiao, X. Meng, B. Liu: Full inhibition of Whangkeumbae pear polyphenol oxidase enzymatic browning reaction by l-cysteine. In: Food chemistry. Band 266, November 2018, S. 1–8, doi:10.1016/j.foodchem.2018.05.086, PMID 30381163.
- ↑ S. Wu: Glutathione suppresses the enzymatic and non-enzymatic browning in grape juice. In: Food chemistry. Band 160, Oktober 2014, S. 8–10, doi:10.1016/j.foodchem.2014.03.088, PMID 24799201.
- ↑ C. Billaud, C. Maraschin, M. N. Peyrat-Maillard, J. Nicolas: Maillard reaction products derived from thiol compounds as inhibitors of enzymatic browning of fruits and vegetables: the structure-activity relationship. In: Annals of the New York Academy of Sciences. Band 1043, Juni 2005, S. 876–885, doi:10.1196/annals.1333.099, PMID 16037314.
- ↑ H. Nie, L. Liu, H. Yang, H. Guo, X. Liu, Y. Tan, W. Wang, J. Quan, L. Zhu: A Novel Heptapeptide with Tyrosinase Inhibitory Activity Identified from a Phage Display Library. In: Applied biochemistry and biotechnology. Band 181, Nummer 1, Januar 2017, S. 219–232, doi:10.1007/s12010-016-2208-3, PMID 27639393.
- ↑ Y. F. Lin, Y. H. Hu, H. T. Lin, X. Liu, Y. H. Chen, S. Zhang, Q. X. Chen: Inhibitory effects of propyl gallate on tyrosinase and its application in controlling pericarp browning of harvested longan fruits. In: Journal of agricultural and food chemistry. Band 61, Nummer 11, März 2013, S. 2889–2895, doi:10.1021/jf305481h, PMID 23427826.
- ↑ W. Y. Lim, C. W. Wong: Inhibitory effect of chemical and natural anti-browning agents on polyphenol oxidase from ginger (Z Roscoe). In: Journal of food science and technology. Band 55, Nummer 8, August 2018, S. 3001–3007, doi:10.1007/s13197-018-3218-7, PMID 30065409, PMC 6045987 (freier Volltext).
- ↑ D. Redondo, M. E. Venturini, R. Oria, E. Arias: Inhibitory effect of microwaved thinned nectarine extracts on polyphenol oxidase activity. In: Food chemistry. Band 197, Pt April 2016, S. 603–610, doi:10.1016/j.foodchem.2015.11.009, PMID 26616994.
- ↑ K. F. Schulbach, J. V. Johnson, A. H. Simonne, J. M. Kim, Y. Jeong, Y. Yagiz, M. R. Marshall: Polyphenol oxidase inhibitor from blue mussel (Mytilus edulis) extract. In: Journal of food science. Band 78, Nummer 3, März 2013, S. C425–C431, doi:10.1111/1750-3841.12059, PMID 23425135.
- ↑ M. Friedman: Prevention of adverse effects of food browning. In: Advances in Experimental Medicine and Biology. Band 289, 1991, S. 171–215, PMID 1897392.
