Sulfite

Sulfite sind die Salze und Ester der Schwefligen Säure H2SO3. Die Salze enthalten als Anion das Sulfition (SO32−). Sie werden häufig als Konservierungsmittel in Wein, Trockenobst und Kartoffelprodukten eingesetzt. Sulfite treten allerdings auch natürlich in nahezu allen Weinen auf.
Ebenfalls als Sulfite bezeichnet werden die Ester der Schwefligen Säure mit der allgemeinen Formel R-O-S(=O)-O-R′ (mit R und R′ als organische Reste).
Die Schweflige Säure ist eine zweiprotonige Säure. Daher existieren unter den Salzen die
- Sulfite (MI2SO3), die auch normale, neutrale oder sekundäre Sulfite genannt werden und
- Hydrogensulfite (MIHSO3), die auch primäre oder saure Sulfite oder Bisulfite genannt werden.
Hydrogensulfite sind als feste Salze nicht existent und liegen nur in wässrigen Lösungen vor. Beim Einengen einer Lösung reagieren Hydrogensulfite unter Wasserabspaltung und Bildung einer Schwefel-Schwefel-Bindung zu Disulfiten (S2O52−):

Unter sauren Bedingungen setzen Sulfite und Hydrogensulfite Schwefeldioxid frei:
Verwendung
Sulfite werden als Reduktionsmittel eingesetzt. Das Hydrogensulfit-Anion reagiert in chemischen Reaktionen als Nukleophil (z. B.: mit Aldehyden unter Bildung gut kristallisierender Salze). Wichtige Verfahren zur Herstellung von Zellstoff und Papier aus Holz arbeiten mit Sulfiten, siehe Sulfitverfahren (unter allem Calciumhydrogensulfit, nach Mitscherlich).
Sulfite im Wein
Die Kennzeichnung „enthält Sulfite“ bzw. „enthält Schwefeldioxid“ ist nach Art. 3 Abs. 3 der Wein-Marktorganisations-Durchführungsverordnung[1] bei Konzentrationen von mehr als 10 mg/l verbindlich vorgeschrieben. In den USA müssen Weine, die nach Mitte 1987 abgefüllt wurden, einen Hinweis auf Sulfite auf dem Etikett enthalten. Die entsprechende Regulierung in der EU gilt seit 2005. Die Kennzeichnungspflicht geht darauf zurück, dass Menschen mit einer Überempfindlichkeit gegen Sulfite bei Konsum auch geringer Mengen Sulfit Unverträglichkeitsreaktionen wie z. B. Bronchospasmen und Asthma, anaphylaktoide Reaktionen, Urticaria und niedrigen Blutdruck zeigen.[2]

Sulfite entstehen in geringen Mengen (10–30 mg/l) auf natürliche Weise während der alkoholischen Gärung des Weines. Seit dem Ende des 18. Jahrhunderts ist die antimikrobielle sowie die antioxidative Wirkung des Schwefels bekannt. Seit dieser Zeit ist der Zusatz von Schwefel in der weltweiten Weinherstellung fest verankert. In Wein werden Mengen an Schwefeldioxid zwischen 90 und 400 mg/l verwendet. Schwefeldioxid (SO2) wird dem Wein gasförmig, in wässriger Lösung, als „Schwefelpulver“ (Kaliumdisulfit), in Form von Tabletten oder, wie früher, durch Ausbrennen von Fässern mit Schwefelspänen zugesetzt.
Sulfite ermöglichen, Weine über längere Zeit zu lagern, ohne dass die Weine durch Oxidation komplett „umkippen“, also der Genuss nur noch eingeschränkt oder gar nicht möglich ist. Außerdem verhindern sie unerwünschte Nachgärungen in der abgefüllten Flasche bei restsüßen Weinen, da sie Mikroorganismen (wie z. B. Hefen) effektiv an ihrer Arbeit hindern.
Die Zugabe von Sulfiten ist auch bei Weinen aus ökologischem Anbau zulässig und muss ebenfalls auf der Flasche gekennzeichnet werden.
Es gibt mancherorts Bestrebungen innerhalb der Weinbranche, Weine ohne Zusatz von Schwefeldioxid herzustellen. Vereinzelten konventionellen sowie auch Bioweingütern gelingt dies seit einigen Jahren mit Erfolg, was hauptsächlich der modernen Keltertechnologie zu verdanken ist.
Für Schwefeldioxid im Wein existieren nach EG-VO Höchstgrenzen.[1]
| Art des Weines | EG-Höchstgrenze SO2 gesamt |
|---|---|
| Rotwein < 5 g/l Restzucker | 150 mg/l (bis 31. Juli 2009: 160 mg/l) |
| Rotwein > 5 g/l Restzucker | 200 mg/l (bis 31. Juli 2009: 210 mg/l) |
| Weißwein & Roséwein < 5 g/l Restzucker | 200 mg/l (bis 31. Juli 2009: 210 mg/l) |
| Weißwein & Roséwein > 5 g/l Restzucker | 250 mg/l (bis 31. Juli 2009: 260 mg/l) |
| Spätlese und vergleichbare ausländische Weine | 300 mg/l |
| Auslese und vergleichbare ausländische Weine | 350 mg/l |
| Beerenauslese und Trockenbeerenauslese, Eiswein und vergleichbare ausländische Weine | 400 mg/l |
| Weine mit dem Hinweis „für Diabetiker geeignet“ (seit dem 1. Juli 2007 nicht mehr erlaubt) | 150 mg/l |
DNA-Methylierung
Bisulfite können selektiv mit Cytosinen in DNA reagieren. Dies wird bei der Bisulfit-Sequenzierung zur Bestimmung methylierter DNA verwendet.
Nachweis
Der qualitative Nachweis kann indirekt mit Permanganaten erfolgen. Diese entfärben sich in einer Redoxreaktion, wenn Sulfite zugegen sind.
- Sulfit-Ionen reagieren mit Permanganat-Ionen in saurer Umgebung zu Mangan(II)-Ionen, Sulfat-Ionen und Wasser.
Die Reaktion ist nicht spezifisch für Sulfite und kann daher nur als Nachweis für Sulfite verwendet werden, wenn die Anwesenheit anderer Reduktionsmittel ausgeschlossen ist. Ebenso wird eine Iodlösung von Sulfiten entfärbt, wobei Iod zu Iodid reduziert und Sulfit zu Sulfat oxidiert wird.
Mit Nitroprussid-Natrium bildet sich in Anwesenheit von Zinkionen ein roter Niederschlag von Zn2[Fe(CN)5SO3].[3] Mit Bariumchloridlösung bildet sich ein weißer Niederschlag von Bariumsulfit, der im Unterschied zu Bariumsulfat leicht in Säuren löslich ist.[4]
Beispiele
Salze der Schwefligen Säure sind
- Kaliumsulfit
- Natriumsulfit
- Magnesiumsulfit
- Natriumhydrogensulfit (Natriumbisulfit)
- Calciumhydrogensulfit (Calciumbisulfit).
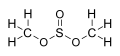
Ester der Schwefligen Säure sind
- Albertiniit (Fe2+(SO3)·3H2O)
- Fleisstalit (Fe2+(SO3)·3H2O)
- Hannebachit (Ca(SO3)·0,5H2O)
- Kollerit ((NH4)2Fe3+(SO3)2(OH)·H2O)
- Mikenewit (Mn2+(S4+O3)·3H2O)
Siehe auch
Literatur
- Pascal Ribéreau-Gayon, Denis Dubourdieu, Bernard Donèche, Aline Lonvaud u. a.: Traité d’oenologie, 1. Microbiologie du vin, Vinifications. Dundo, Paris 2004, ISBN 2-10-007301-X.
Weblinks
Einzelnachweise
- ↑ a b Verordnung (EG) 753/2002 der Kommission vom 29. April 2002, Volltext
- ↑ Bundesinstitut für Risikobewertung: Stark überhöhte Gehalte an Schwefeldioxid in Wein. (PDF; 108 kB) 13. November 2003.
- ↑ Hans Peter Latscha, Gerald W. Linti, Helmut Alfons Klein: Analytische Chemie, Springer, Berlin, 4. Aufl., 2004, S. 52 Google Books
- ↑ Jander/Blasius: Lehrbuch der analytischen und präparativen anorganischen Chemie, 5. Auflage, S. Hirzel, Stuttgart-Leipzig 1965, S. 132–133.
- ↑ Malcolm Back, Cristian Biagioni, William D. Birch, Michel Blondieau, Hans-Peter Boja und andere: The New IMA List of Minerals – A Work in Progress – Updated: July 2024. (PDF; 3,6 MB) In: cnmnc.units.it. IMA/CNMNC, Marco Pasero, Juli 2024, abgerufen am 13. August 2024 (englisch).

![{\displaystyle \mathrm {2\ HSO_{3}^{-}\ \rightleftharpoons \ [O_{2}S{-}SO_{3}]^{2-}+H_{2}O} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/36494f459b9058c12aa7344a18ea3ce5d8c7cb5e)

