Photopolymer
Ein Photopolymer ist ein Polymer, das seine Eigenschaften ändert, wenn es mit Licht aus dem UV-VIS-Bereich des elektromagnetischen Spektrums bestrahlt wird.[1] Es handelt sich um strukturelle Änderungen, wie z. B. die photochemische Härtung des Materials durch Vernetzung. Das unten genannte Beispiel zeigt eine Mischung aus Monomeren, Oligomeren und Photoinitiatoren, das sich bei einer Photopolymerisation in ein gehärtetes Material umwandelt.[2][3]
Es gibt eine breite Vielfalt technologisch nützlicher Anwendungen für Photopolymere, so gibt es beispielsweise Farben, Zahnfüllungen und Lacke, die bei der Härtung auf lichtabhängiger Polymerisierung basieren. In manchen Fällen können Brüche photochemisch in Sekunden repariert werden, für die man bei thermischer Erwärmung eine halbe Stunde oder länger braucht.[4] Reparaturmaterialien werden oft verwendet in der Medizintechnik, in Druckereien und in der Photoresisttechnik.

Photopolymere zählen zu den Funktionspolymeren.
Eigenschaften
Änderungen der strukturellen und chemischen Eigenschaften können intern durch Chromophore, die die Polymereinheit schon besitzt, oder extern durch Zugabe von Photosensibilisatoren hervorgerufen werden. Ein typisches Photopolymer besteht aus einer Mischung multifunktioneller Monomere und Oligomere, die polymerisieren, und zu diesem Zweck sind eine Vielfalt von solchen Molekülen entwickelt worden, die bei Licht (oder bei Anwesenheit eines anderen Radikalstarters) polymerisieren. Photopolymere unterliegen einem Prozess der Photohärtung bzw. Aushärtung, wobei die Oligomere, die dem Licht ausgesetzt werden, vernetzen oder verzweigen. Das Resultat ist ein Netzwerk von Polymeren. Ein Vorteil der Photohärtung ist, dass sie selektiv eingesetzt werden kann, wenn man als Lichtquelle Laser verwendet. Oft sind jedoch Photoinitiatoren erforderlich, um die Polymerisation zu starten. Diese sind Verbindungen, die bei Bestrahlung mit Licht in reaktive Moleküle zerfallen, die als Radikale die Polymerisation der einzelnen Oligomere in Gang bringen.[5] Ein Beispiel für eine Mischung, die vernetzt, wenn sie belichtet wird, ist unten gezeigt. Sie besteht aus dem Monomer Styrol und dem Oligomer Acrylat.[6]

Meistens werden Photopolymer-Systeme durch UV-Licht gehärtet, da es energiereicher ist als sichtbares Licht, jedoch wurden schon Farbstoff-basierte Photoinitiator-Systeme für sichtbares Licht entwickelt, die den Vorteil haben, dass sie einfacher und sicherer zu handhaben sind.[7] UV-Härtung hat in industriellen Prozessen über die letzten Jahrzehnte beträchtlich an Bedeutung gewonnen. Viele thermische und lösungsmittelbasierte Technologien sind durch die Photopolymerisation ersetzt worden. Vorteil der Photochemie sind ein hoher Polymerisationsgrad und bessere Umweltverträglichkeit gegenüber der Verwendung von leicht flüchtigen organischen Lösungsmitteln. Für den Start der Photopolymerisierung gibt es zwei verschiedene Mechanismen: radikalisch und ionisch.[1][4] Die generelle Reaktion besteht darin, das Polymer mit einer kleinen Menge Photoinitiator zu versetzen, gefolgt von einer selektiven Bestrahlung mit Licht, was zu einem stark vernetzten Produkt führt. Für die meisten derartigen Reaktionen ist es nicht notwendig, ein Lösungsmittel zu verwenden, so dass Reaktionen des Initiators mit dem Lösungsmittel und somit Verunreinigungen verhindert werden, zusätzlich werden die Gesamtkosten gesenkt.[1][4]
Mechanismen
Ionischer Mechanismus
Im ionischen Härtungsprozess wird ein Photoinitiator verwendet, um eine funktionelle Gruppe eines Oligomers zu aktivieren, so dass es vernetzen kann. Typischerweise ist die Photopolymerisation ein selektiver Prozess und es ist entscheidend, dass sie nur dort stattfindet, wo es vorgesehen ist. Diese lösungsmittelfreie Reaktion wird unter Zusatz eines anionischen oder kationischen Photoinitiators ausschließlich bei Bestrahlung mit Licht durchgeführt. Monomere, die für die kationische Polymerisation verwendet werden, sind: Styrol, Vinylether, N-Vinyl-Carbazole, Lactone, Lactame, cyclische Ether, cyclische Acetale und cyclische Siloxane. Die Mehrzahl der ionischen Photoinitiatoren sind Kationen, die Anionen sind weniger erforscht.[5] Es gibt eine Reihe von kationischen Initiatoren: Oniumsalze, Organometallverbindungen und Pyridiniumsalze.[5] Wie oben erwähnt, ist einer der Nachteile von Photoinitiatoren, dass sie dazu tendieren, Licht aus dem UV-Bereich zu absorbieren.[7] Photosensibilisatoren oder Chromophore, die Licht einer viel kürzeren Wellenlänge absorbieren, können verwendet werden, um den Photoinitiator durch Energietransfer photochemisch anzuregen.[5] Eine andere Variation dieses Reaktionstyps ist die radikalgestützte kationische Polymerisation. In diesem Fall reagiert ein freies Radikal mit dem Photoinitiator, um die Polymerisation zu starten. Die meisten industriell verwendeten Verbindungen sind hierbei Epoxide, Oxetane und Vinylether.[8] Einer der Vorteile der kationischen Photopolymerisation ist, dass die Polymerisation nicht mehr sauerstoffempfindlich ist und daher keine Inertgasatmosphäre erforderlich ist.[1]
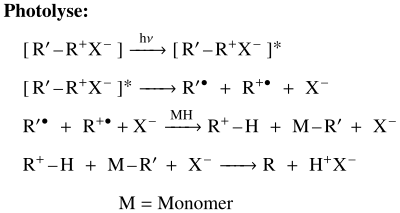
Kationische Photoinitiatoren
Der vorgeschlagene Mechanismus für kationische Polymerisation beginnt mit der Anregung des Photoinitiators. Beides, die homolytische Spaltung und die Dissoziation eines Gegenanions finden gleichzeitig statt, so dass ein Radikalkation (R+), ein Arylradikal (R´) und ein Anion (X-) erzeugt werden. Die Entfernung einer Lewissäure (im Bild oben ein Wasserstoff), von einem Radikalkation (R) produziert ein schwach gebundenes Proton und ein freies Radikal. Die Säure wird später deprotoniert durch das Anion in der Lösung, indem es eine Lewissäure mit dem Startanion(X-) als Gegenion bildet. Man vermutet, dass schließlich das Säureproton die Polymerisation hervorruft.[9]
Onium-Salze
Seit ihrer Entdeckung im Jahr 1970 haben Aryl-Onium-Verbindungen, insbesondere Iodonium- und Sulfoniumsalze, an Bedeutung gewonnen und fanden Anwendung in industriellen Prozessen. Andere, weniger gebräuchliche Onium-Salze, die hier nicht weiter erwähnt werden, sind beispielsweise Ammonium- und Phosphonium-Salze.[8]
| Onium-Salze |
|---|
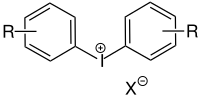
Iodonium-Salz |

Sulfonium-Salz |
| Zur Bedeutung von R und X: Siehe Begleittext. |
Die typische Onium-verbindung, die als Photoinitiator verwendet wird, enthält zwei oder drei Arylgruppen für Iodonium und für Sulfonium entsprechend. Onium-Salze absorbieren generell Licht im UV-Bereich von 225 bis 300 nm.[10] Ein entscheidendes Merkmal für die Eignung des Onium-Salzes als Photoinitiator ist, dass das zentrale Anion nicht nucleophil ist. Die im ersten Reaktionsschritt entstehende Säure ist der Radikalstarter für die Polymerisation. Eine mögliche Schlussreaktion der Kettenreaktion wäre, wenn anstelle einer funktionellen Gruppe des Oligomers das Zentralion der Oniumverbindung als Nucleophil reagiert.
Metallorganische Verbindungen
Obwohl weniger gebräuchlich, können auch Übergangsmetall-Komplexe als kationische Photoinitiatoren reagieren. Generell ist der Mechanismus einfacher als der für Onium-Salze oben beschriebene. Die meisten Photoinitiatoren bestehen aus einem Metall-Salz mit einem nicht-nucleophilen Zentralanion. Zum Beispiel sind Ferrocene sehr wichtig für kommerzielle Anwendungen.[11] Die Absorptionsbande für Ferrocen-Komplexe liegt im sichtbaren Bereich des Spektrums. Bei der Belichtung verliert das Metallzentrum einen Liganden, der ersetzt wird durch eine funktionelle Gruppe, wodurch die Polymerisation beginnt. Ein Nachteil dieser Methode ist die Empfindlichkeit gegenüber Sauerstoff. Es gibt einige metallorganische Photoinitiatoren, die nach ähnlichen Mechanismen reagieren. Bei der anionischen Polymerisation ist die photochemische Anregung des Zentralatoms gefolgt von einer Bindungsspaltung oder von einem Elektronentransfer, der das aktive Anion, den Photoinitiator, erzeugt.[5]
Pyridin-Salze
Generell werden solche Pyridine als Photoinitiatoren verwendet, die N-substituiert sind und eine positive Ladung am Stickstoffatom tragen. Das Zentralion ist ein nicht-nucleophiles Anion. Bei Bestrahlung findet eine homolytische Bindungsspaltung statt, die ein Pyridinradikalkation und ein freies Radikal erzeugt. Meistens wird durch das Prydinradikal ein Wasserstoffatom von dem Oligomer entfernt. Das so erzeugte freie Radikal wird abgefangen von einem Radikal in der Lösung. Es resultiert eine starke Pyridinsäure, die als Radikalstarter die Polymerisation in Gang bringt.[12]
Radikalischer Mechanismus
Bevor der radikalische Mechanismus der Polymerisierung aufgeklärt wurde, beobachtete man, dass bestimmte Monomere bei Belichtung polymerisieren. Danach fand man heraus, dass sich viele Verbindungen durch Licht spalten lassen und verwendete sie als Photoinitiator (Starter) bei der Polymerherstellung.[1] Beim radikalischen Mechanismus UV-härtender Systeme wird Licht durch den Photoinitiator absorbiert, der freie Radikale erzeugt, die zur Vernetzung einer Mischung aus funktionalisierten Monomeren und Oligomeren führt, wodurch ein Polymerfilm oder Fotolack entsteht.[13] Photohärtende Materialien denen ein radikalischer Mechanismus zugrunde liegt, verlaufen in einer Kettenreaktion, die aus drei prinzipiellen Schritten besteht:
- Startreaktion (Initiation)
- Kettenwachstum (Propagation)
- Kettenabbruch (Termination)
Diese drei Schritte werden im folgenden Schema skizziert, wobei R• das Radikal ist, das bei der Startreaktion durch Licht erzeugt wird, und M das Monomer.[4] Das aktive Monomer wird in einer Radikalreaktion gebildet, dabei wächst es zu einer radikalischen Polymerkette. In UV-härtenden Materialien bedeutet der Wachstumsschritt, dass die Kettenradikale mit reaktiven Doppelbindungen der Oligomere reagieren. Die Schlussreaktion kommt dadurch zustande, dass zwei Kettenradikale aufeinandertreffen (Kombination), oder dadurch, dass ein Wasserstoffatom auf eine andere Radikalkette übertragen wird (Disproportionierung), so dass zwei Polymerketten entstehen.

Die meisten Gemische, die durch Kettenwachstum aushärten, enthalten eine Mischung aus Momomeren und Oligomeren mit einer molaren Masse von 500 bis 3000 u. Generell haben Monomere mit einer höheren Funktionalität eine stärkere Vernetzungsdichte des fertigen Polymerfilms.[5] Typischerweise absorbieren die Monomere und Oligomere nicht genügend Energie aus den verwendeten Lichtquellen oder nicht im passenden Wellenlängenbereich, weshalb Photoinitiatoren zugefügt werden.[4][13]
Photoinitiatoren
Es gibt zwei Arten von Photoinitiatoren, die freie Radikale erzeugen: Ein Zwei-Komponenten-System, wo das Radikal durch Abtrennung eines Wasserstoffatoms von einer Donor-Verbindung erzeugt wird, und ein Ein-Komponenten-System, wo zwei Radikale durch Bindungsspaltung erzeugt werden:[13]
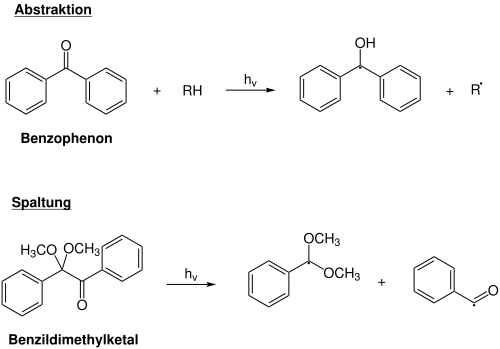
Benzophenon, Xanthon und Chinon sind Beispiele für den ersten Typ mit aliphatischen Aminen als Donor-Komponente. Das erzeugte Radikal R• wird der Radikalstarter im Polymerisationsprozess.
Benzoylether, Acetophenon, Benzoyloxim und Acylphosphin sind Beispiele für bindungsspaltende Photoinitiatoren. Durch die Bindungsspaltung erfolgt typischerweise die Erzeugung zweier Radikale bei der Lichtabsorption, und beide Radikale können die Polymerisation starten. Dieser Typ Radikalstarter erfordert keine weiteren Zusätze, wie beispielsweise aliphatische Amine. Dies ist vorteilhaft, da die Kettenlänge und Vernetzungsdichte des resultierenden Polymerfilms nicht durch weitere Zusätze reduziert wird.
Oligomere und Monomere
Die Eigenschaften des photogehärteten Materials, wie Flexibilität, Haftung und chemische Beständigkeit, basieren auf den im photogehärteten Gemisch vorhandenen Oligomeren. Oligomere sind typischerweise Epoxide, Polyurethane, Polyether oder Polyester, von denen alle Komponenten die spezifischen Materialeigenschaften des resultierenden Produktes verursachen. Im gezeigten Beispiel wird ein Epoxy-Oligomer verwendet, funktionalisiert durch ein Acrylat. Acyl-epoxide sind nützliche Lacke für Metalle. Acyluretan-Oligomere sind typischerweise flexibel und die idealen Lacke für Fußböden, Druckplatten und Verpackungsmaterialien. Acrylierte Polyether und Polyester erzeugen schwer säurelösliche Filme, sind jedoch unbeständig gegenüber UV-Licht und können daher nicht als UV-härtendes Material verwendet werden. Oft werden die Reaktionsmischungen aus unterschiedlichen Oligomeren hergestellt, um die passenden Materialeigenschaften zu erzeugen.[4]

Die Monomeren für UV-härtende Substanzen kontrollieren die Härtungsgeschwindigkeit, die Vernetzungsdichte, die Oberflächeneigenschaften des Polymerfilms und die Viskosität des Granulats. Beispiele für Monomere sind Styrol, N-Vinylpyrrolidon und Acrylat. Styrol ist ein preiswertes Monomer, das schnell härtet, N-Vinylpyrrolidon besitzt eine hohe Flexibilität und ist mindergiftig, und Acrylate sind sehr reaktiv, härten schnell und sind vielseitig verwendbar (mit Monomeren von mono- bis tetrafunktional.) Die Monomere machen, wie die Oligomere, die gewünschten Eigenschaften des Endproduktes aus.[4]
Anwendungen
Photopolymerisation ist eine weit verbreitete Technologie, die angewandt wird für bildgebende Verfahren bis zu biomedizinischen Anwendungen.
Medizinische Verwendung
Zahnmedizin ist ein Markt, wo radikalische Polymerisation breite Anwendung findet als Klebstoff oder als Material für Zahnfüllungen und Schutzlacke. Diese Zahnfüllungen basieren auf Campherchinon als Initiator, einer Matrix aus Methacylat-Oligomeren und einem anorganischen Füllstoff, wie Siliziumdioxid. UV-härtende Klebstoffe werden auch verwendet bei der Produktion von Kathetern, Hörgeräten, Atemmasken, medizinischen Filtern und Sensoren zur Blutanalyse.[1] Photopolymere wurden auch für den Wirkstofftransport, für Gewebeherstellung und für Zellkapseln verwendet.[14] Photopolymerisationsprozesse für diese Anwendungen werden in vivo oder ex vivo durchgeführt. In vivo Photopolymerisation hätte den Vorteil der Verwendung für Produktion und Implantation bei minimalinvasiven Eingriffen. Ex vivo Photopolymerisation würde die Herstellung komplexer Matrices und deren vielseitige Verwendung ermöglichen. Obwohl Photopolymere eine weite Bandbreite neuer biomedizinischer Anwendungen bietet, muss die Biokompatibilität noch getestet und entwickelt werden.
3D-Bildgebung
Stereolithographie, digitale Bildgebung und 3D-Tintenstrahl-Druck sind nur einige 3D-Techniken, bei denen Photopolymere verwendet werden. 3D-Bildgebung wird normalerweise mit computergestützten Technologien durchgeführt, wie z. B. Software, die ein 3D-Bild in ein plastisches 3D-Objekt umwandelt. 3D-Bildgebung wird normalerweise mit Software durchgeführt, die ein 3D-Bild erzeugt, das dann in einen plastischen dreidimensionalen Körper umgewandelt wird. Das Bild wird in Scheiben geschnitten, wobei jede Scheibe unter UV-Härtung des flüssigen Polymers kopiert wird und so das Bild in ein festes Objekt umwandelt. Photopolymere für die 3D-Bildgebung werden so entwickelt, dass sie eine geringe Volumenabnahme bei der Polymerisation haben, um ein Schrumpfen des festen Objekts zu verhindern. Die normalerweise für 3D-Bildgebung verwendeten Monomere sind multifunktionelle Acrylate und Methacrylate, kombiniert mit einer nicht-polymerisierenden Verbindung, um Volumenschrumpfung zu verhindern. Eine passend zusammengesetzte Mischung von Epoxiden mit kationischen Photoinitiatoren wird in zunehmendem Maße verwendet, da die Volumenabnahme bei der Ringöffnung des Epoxids signifikant geringer ist als die der Acrylate und Methacrylate. Radikalisch und kationisch polymerisierende Mischungen, die Epoxide und Acrylat-Monomere enthalten, werden auch verwendet, wodurch man hohe Polymerisationsraten durch die Acrylatkomponente und sehr gute mechanische Eigenschaften durch die Epoxidmatrix gewinnt.[1]
Photoresists
Photoresists sind Fotolacke oder Oligomere, die auf eine Oberfläche aufgetragen werden und so hergestellt sind, dass sie ihre Eigenschaften nach Belichtung verändern. Diese Veränderung bedeutet die Photohärtung eines flüssigen Oligomers zu einer unlöslichen Netzstruktur als Fotolack (negativer Lack) oder umgekehrt die Zersetzung eines festen Polymers in flüssige Produkte (positiver Lack). Beides hat viele Anwendungen beim Design und der Produktion von Mikrochips. Die Möglichkeit, einen Lack herzustellen, indem man eine Lichtquelle verwendet, führte zur Anwendung bei der Photolithographie.

Negative Resists
Wie oben erwähnt, sind Negativ-Resists Photopolymere, die bei Bestrahlung zu unlöslichen Lacken werden. Für sie gibt es ein breites Anwendungsgebiet, insbesondere beim Design und bei der Herstellung von elektronischen Mikrochips. Charakteristisch für die Fotolacke ist die Anwesenheit funktioneller Gruppen an den verwendeten Polymeren. Aus dem mit UV-Licht bestrahlten Polymer resultiert in Anwesenheit eines Photoinitiators ein chemisch stabiles Polymer-Netzwerk. Eine gebräuchliche funktionelle Gruppe für einen Fotolack ist ein Epoxid.[15]
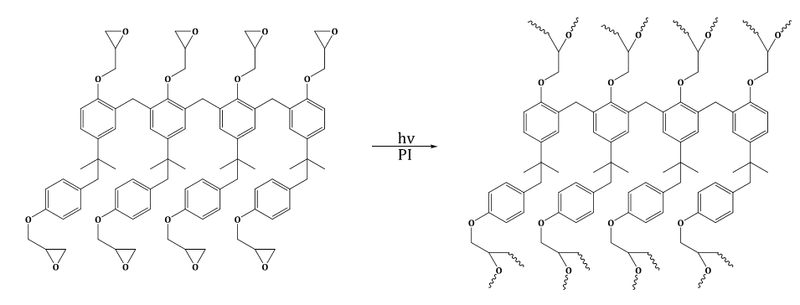
Dies ist ein Beispiel für intramolekulare Polymerisation, bei der eine Matrix aus einem verzweigten Material gebildet wird.
Positive resists
Wie bereits erwähnt, ändern positive Resists bei Bestrahlung ihre chemische Struktur und werden flüssig, (oder besser löslich). Die Strukturänderung basiert auf einem Bindungsbruch innerhalb des polymeren Netzes. Das durch die Bestrahlung zersetzte Polymer kann mit einer Entwicklerlösung weggewaschen werden, stehen bleibt das unbelichtete Polymer. Diese Technik erlaubt die Herstellung sehr feiner Schablonen für die Mikroelektronik.[16] Für diese Anwendungen braucht ein positiver Resist Polymere mit leicht spaltbaren Verzweigungen und einen Photoinitiator, der Bindungen im Polymer öffnet. Ein Polymer, das sich bei Bestrahlung verflüssigt oder zu einem löslichen Produkt wird, wird verwendet als positiver Photoresist. Polymere, deren funktionelle Gruppen durch einen photochemisch erzeugten Katalysator hydrolysiert werden, sind beispielsweise Polycarbonate und Polyester.[17]
Feindruck

Photopolymere können verwendet werden, um Druckplatten herzustellen, mit denen man dann auf Papier drucken kann, wie mit metallischen Druckplatten.[18] Diese Technik wird oft für den Zeitungsdruck verwendet, um Buchstaben dreidimensional erscheinen zu lassen. Das Design kann am Computer entworfen werden, ohne dass man es in Metall einritzen muss. Es wird oft für Visitenkarten verwendet.[19][20]
Einzelnachweise
- ↑ a b c d e f g Elsa Reichmanis, James Crivello: Photopolymer Materials and Processes for Advanced Technologies. In: Chem. Mater. Band 26, 2014, S. 533–548.
- ↑ Roger Phillips: Photopolymerization. In: Journal of Photopolymerization. Band 25, 1984, S. 79–82, doi:10.1016/0047-2670(84)85016-9.
- ↑ Jeff Burton: A Primer on UV-Curable Inkjet Inks. Specialty Graphic Imaging Association, archiviert vom (nicht mehr online verfügbar) am 6. August 2020; abgerufen am 7. August 2017.
- ↑ a b c d e f g A. Ravve: Light-Associated Reactions of Synthetic Polymers. Springer Science+Business Media, New York 2006, ISBN 0-387-31803-8.
- ↑ a b c d e f Jean Pierre Fouassier: Photoinitiators for Polymer Synthesis: Scope, Reactivity and Efficiency. Wiley-VCH Verlag, Weinheim 2012, ISBN 978-3-527-64824-5.
- ↑ Radiation Chemistry in EB-and UV-Light Cured Inks. Paint & Coatings Industry, abgerufen am 7. August 2017.
- ↑ a b J. P. Fouassier, X.Allonas, D. Burget: Photopolyermziation reactions under visible lights: principle, mechanisms and examples of applications. In: Progress in Organic Coatings. Band 47, 2003, S. 16–36, doi:10.1016/S0300-9440(03)00011-0.
- ↑ a b J. Crivello, E. Reichmanis: Photopolymer Materials and Processes for Advanced Technologies. In: Chemistry of Materials. Band 26, 2014, S. 533–548, doi:10.1021/cm402262g.
- ↑ Viktor Zhdankin: Hypervalent Iodine Chemistry: Preparation, Structure, and Synthetic Applications of Polyvalent Iodine Compounds. John Wiley & Sons, 2013, S. 427.
- ↑ Jean Fouassier: Photoinitiators for Polymer Synthesis: Scope, Reactivity, and Efficiency. John Wiley & Sons, 2012, S. 293.
- ↑ K. Meier: Proceedings of the RadCure Europe. Basle Technical Paper, 1985.
- ↑ Eiji Takahashi, Fumio Sanda, Takeshi Endo: Novel pyridinium salts as cationic thermal and photoinitiators and their photosensitization properties. In: Journal of Polymer Science Part A: Polymer Chemistry. Band 40, Nr. 8, 2002, S. 1037, doi:10.1002/pola.10186.
- ↑ a b c Charles Hoyle: Radiation Curing of Polymeric Materials. Am. Chem. Soc., Washington, DC 1990, S. 1–15.
- ↑ Biancamaria Baroli: Photopolymerization of biomaterials. In: J. Chem. Technol. Biotechnol. Band 81, 2006, S. 491–499, doi:10.1002/jctb.1468.
- ↑ SU-8 Photosensitive Epoxy. Archiviert vom (nicht mehr online verfügbar) am 30. Mai 2012; abgerufen im Jahr 2014.
- ↑ Harry Allcock: Introduction to Materials Chemistry. Wiley and Sons, 2008, ISBN 978-0-470-29333-1, S. 248–258.
- ↑ Larry Thompson: Polymers for Microelectronics. American Chemical Society, 1993.
- ↑ What is a “faux-emboss”? Dolce Press, abgerufen am 24. September 2015.
- ↑ Letterpress polymer plate service. Old City Press, abgerufen am 24. September 2015.
- ↑ What is Letterpress? Baltimore Print Studios, abgerufen am 24. September 2015.
