Calciumpermanganat
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
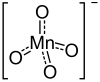
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Calciumpermanganat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | Ca(MnO4)2 | |||||||||||||||
| Kurzbeschreibung |
violetter Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 277,95 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,4 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Calciumpermanganat ist eine chemische Verbindung aus Calcium, Sauerstoff und Mangan. Es ist das Calciumsalz der im freien Zustand unbekannten Permangansäure HMnO4. Für die intensive Färbung des Salzes ist ausschließlich das Permanganat-Anion verantwortlich.
Gewinnung und Darstellung
Calciumpermanganat kann durch Elektrolyse von Lösungen von Alkalimanganaten und Chlorkalk gewonnen werden oder wie beim Magnesiumpermanganat aus Calciumchlorid und Silber- oder Kaliumpermanganat.[1]
Chemische Eigenschaften
Calciumpermanganat Ca(MnO4)2 ist wie Kaliumpermanganat ein starkes Oxidationsmittel.
Verwendung
Calciumpermanganat wird verwendet:
- in der Textilproduktion[1]
- zum Bleichen von Papier
- zur Sterilisierung von Wasser[1] und bei Zahnbehandlungen
- als Katalysator in Raketentreibstoffen
- in Beschichtungen/Flussmitteln von Schweißelektroden[4]
- allgemein als antiseptische, desinfizierende und deodorierende Verbindung
Einzelnachweise
- ↑ a b c d e f g Dale L. Perry: Handbook of Inorganic Compounds. CRC Press, 2016, ISBN 978-1-4398-1462-8, S. 485 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Curt Hunnius: Hunnius Pharmazeutisches Wörterbuch. De Gruyter, 2021, ISBN 978-3-11-242212-0, S. 304 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ HazMap: Calcium permanganate ( vom 11. März 2013 im Internet Archive)

